>>的中率60%以上!今年度の北海道公立高校入試「理科」はここが狙われる!当受験ブログ執筆者の予想出題分野
■ボーダー(合格)ライン・最低点の推移
>>北海道公立高校入試の道コン最低点推移のランク別まとめ
■平均点推移と予想
>>北海道公立高校入試の平均点推移・各科目の正答率・人数分布・平均点予想まとめ
■一般入試の合否判定の手順
>>【最新版】北海道公立高校一般入試の合否判定の手順の詳細まとめ
■一般入試(全体・学区外受験)の最終倍率推移
>>北海道公立高校入試の一般入試(全体・学区外受験)の最終倍率推移
北海道公立高校入試過去問はこちら
★過去問

★模擬テストとリスニング対策

※模擬テストは1教科のみ表示。Amazonなどでは5教科すべて販売されています。
大問1 小問集合
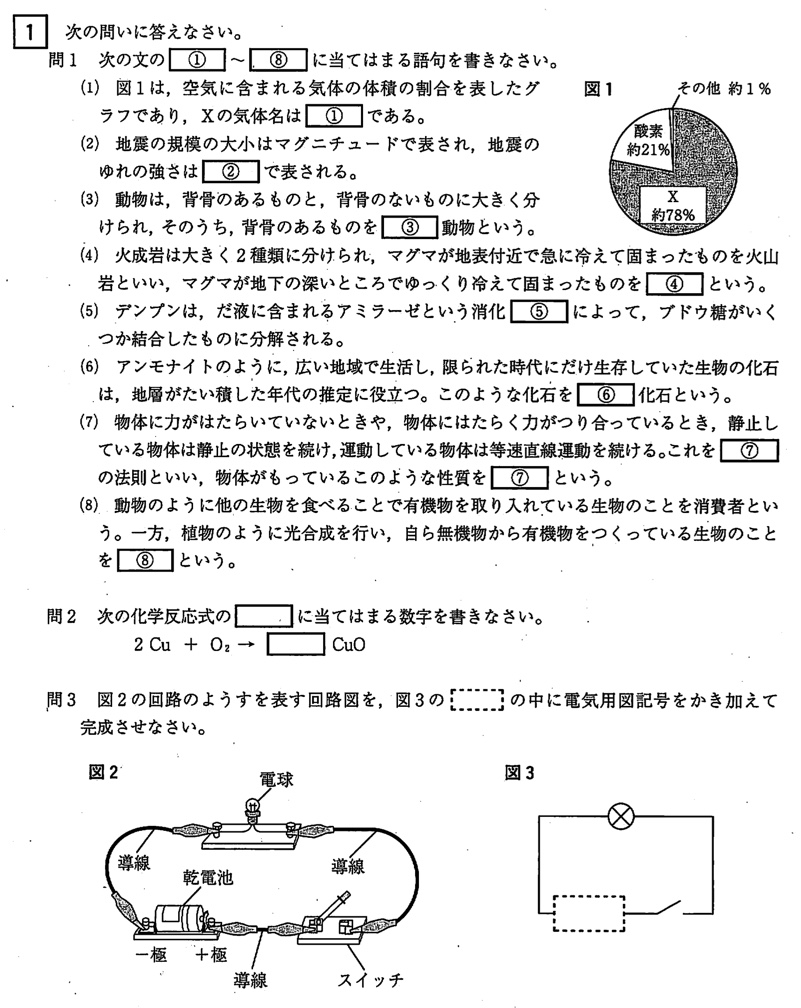
問1
(1)
(答)チッ素
空気中に含まれる気体の体積の割合は、チッ素が約78%、酸素が約21%、アルゴンが約0.9%、二酸化炭素が約0.04%です。
「1位:チッ素、2位:酸素、3位:アルゴン、4位:二酸化炭素」と覚えましょう。
他県の入試問題で、過去に、空気中に含まれる気体の体積の割合が4番目に多い気体(答:二酸化炭素)を問う問題が出題されています。
(2)
(答)震度
地震の規模の大小はマグニチュード、地震の揺れの強さは震度です。
震度は場所によって異なるが、マグニチュードは1つの地震で1つの値となります。
また、マグニチュードは2増えるとエネルギーが1000倍になるよう定められており、マグニチュードが1増えると約32倍になります。
(3)
(答)セキツイ
セキツイ動物と無セキツイ動物の違いを問われています。
セキツイ動物は、魚類・両生類・は虫類・鳥類・ホニュウ類の5つに大別されます。
5つの特徴それぞれについて、詳しく勉強してください。
無セキツイ動物は、まず外骨格の有無で区別し、次に外とう膜の有無で区別していきます。
(4)
(答)深成岩
火成岩は、マグマの冷え方・場所により、火山岩と深成岩に分けられます。
火山岩は「流紋岩・安山岩・玄武岩」の3種類を、深成岩は「花こう岩・せん緑岩・斑れい岩」の3種類を覚えましょう。
これらは、無色鉱物と有色鉱物の割合(二酸化ケイ素の含有量)の違いにより、区分できます。
無色鉱物と有色鉱物の種類(7種類)も押さえてください。
火成岩は粒が角ばっています。
堆積岩と異なり、熱で溶けるため化石が含まれていません。
(5)
(答)酵素
消化酵素として、
炭水化物→ブドウ糖がいくつか結合したものに分解する、アミラーゼ(だ液・すい液)とマルターゼ(小腸の壁)、
タンパク質→アミノ酸に分解する、ペプシン(胃液)とトリプシン(すい液)とペプチターゼ(小腸の壁)、
脂肪→脂肪酸+モノグリセリドに分解する、胆汁(消化酵素なし)とリパーゼ(すい液)
を覚えましょう。
すい液は3大栄養素すべてに作用することも、押さえてください。
(6)
(答)示準
示準化石のキーワードは「時代・年代」、示相化石のキーワードは「自然環境」です。
さらに突っ込んで、示相化石と示準化石の種類も押さえてください。
示準化石だと、三葉虫・フズリナ→古生代、アンモナイト・恐竜→中生代、ビカリア・ナウマンゾウ→新生代、です。
フズリナは堆積岩のひとつ、石灰岩にも含まれています。
フズリナの形も押さえてください。
(7)
(答)慣性
慣性の法則について、この問題文ごと暗記しましょう。
(8)
(答)生産者
生産者と消費者の違いは、問題文のとおりです。
二酸化炭素の流れとして、消費者と分解者は呼吸のみするので一方向の矢印が、生産者である植物は呼吸と光合成の両方をするので両方向の矢印になります。
チッ素の場合は、分解者(根粒菌など)が大気中のチッ素を窒素化合物に合成し、生産者である植物がそれを利用します。
問2
(答)2
化学反応式の係数を合わせる問題です。
左辺はCu原子とO原子が2つずつ、右辺はCu原子とO原子が1つずつなので、CuOの係数は2となります。
問3
乾電池(電源)において、長い方が+極、短い方が−極となります。
電流はプラスの電気で、プラスとプラスは反発し、マイナスとプラスはくっつくので、電流は+極からでて−極に戻るように流れます。
電流の向きは電子の向きと逆です。
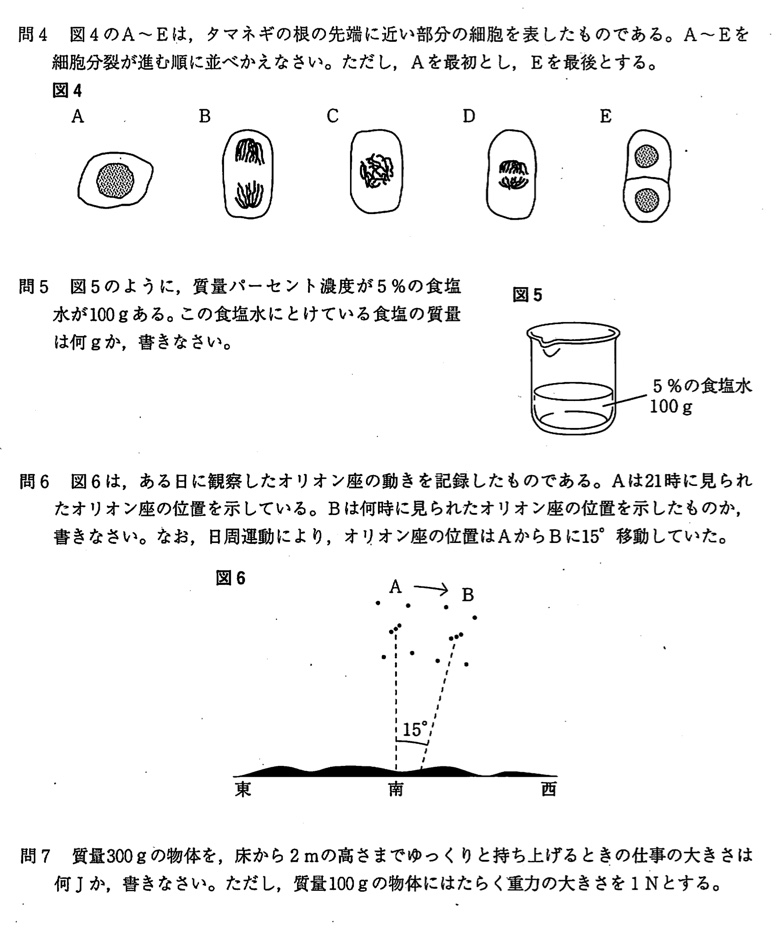
問4
(答)A→C→D→B→E
体細胞分裂の様子について問われています。
間期(A)で染色体が2倍に複製→核膜と核小体が消失(C)→紡錘体が形成され染色体が赤道面に並ぶ(D)→縦裂面で分裂し両極に半分ずつ移動(B)→細胞質分裂(E)
という流れです。
問5
(答)5g
食塩水が100gで濃度が5%なので、かけ算して終わりです。
食塩の質量=100g×(5/100)=5g
問6
(答)22時
星の日周運動の問題です。
南の空では、星は東から西に1時間に15°動いて見えます。
AとBの角度が15°なので、Bの時刻はAの時刻(21時)の1時間後の22時となります。
年周運動だと、1日1°動いて見えるので、15°だと15日なので、15日後にAと同じ時刻に見るとBの位置に見えます。
日周運動と年周運動を組み合わせて、星の位置を把握できるようになってください。
問7
(答)6J
仕事(J)=加えた力(N)×動かした距離(m)、です。
問題文に「物体をゆっくりと持ち上げるとき」とあるので、等速直線運動をしていることが分かります。
等速直線運動では進行方向の力が釣り合うので、加えた力が物体の重力と等しくなります。
仕事(J)=加えた力(N)×動かした距離(m)=物体の重力(N)×動かした距離(m)
あとは上の式に数字を代入して終わりです。
仕事(J)=3N×2m=6J
大問2 植物の生活と種類(生物分野・中1)
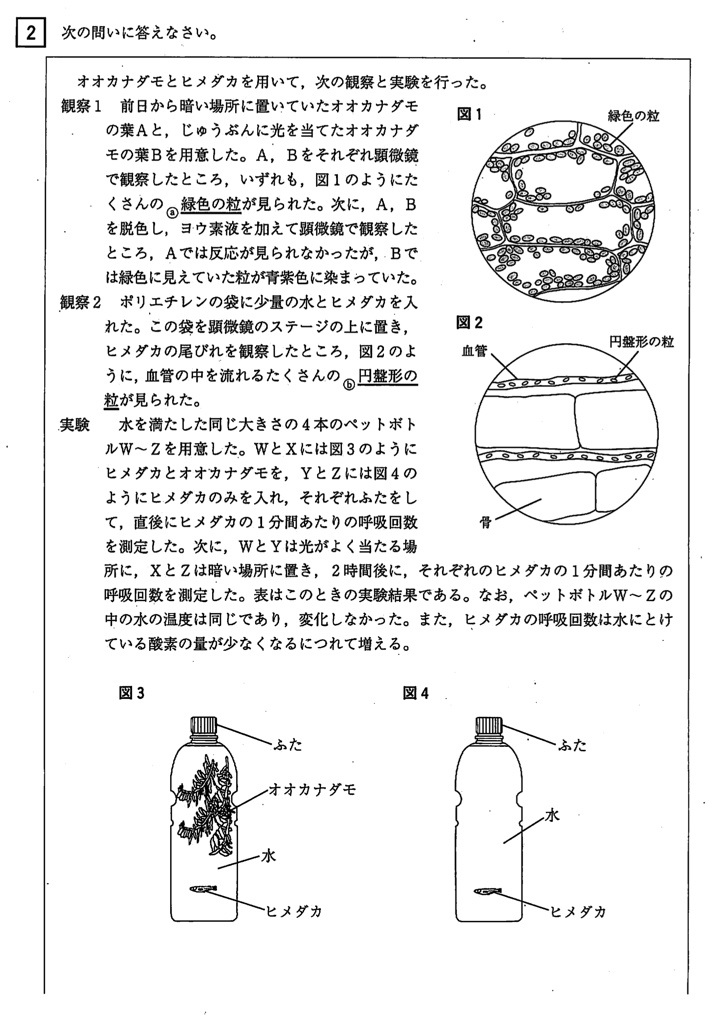

問1(1)
(答)葉緑体
単なる知識問題です。
植物細胞には葉緑体があり、光合成は葉緑体で行われます。
葉緑体は、柵状組織、海綿状組織、気孔の孔辺細胞にあります。
問1(2)
(答)ウ、エ
オオカナダモAとオオカナダモBの違いは、光の有無のみです。
光を当てたオオカナダモBではデンプンが作られたことより、光合成には光が必要であることが分かります(選択肢アOK)。
また、どちらも葉緑体が存在するので、デンプンは葉緑体で作られるとも言えます(選択肢イOK)。
デンプンはヨウ素液と反応して青紫色になるのは常識です。
選択肢ウとエについて、観察1では二酸化炭素も酸素に関するキーワードが一切ないので、ウとエは誤りです。
問2
(答)①ヘモグロビン、②ア、③イ
単なる知識問題です。
ヘモグロビンの性質について、この問題文ごと暗記しましょう。
血液成分には、固形成分の血球(赤血球、白血球、血小板)と液体成分の血しょうがあります。
それぞれの特徴と働きについても押さえてください。
問3(1)
(答)①イ、②ア
①
酸素が発生するのは、オオカナダモが光合成をするからです。
つまり、オオカナダモの有無のみについて問われているので、光が当たっているペットボトルWとYに着目します。
Wは光が当たっているので、オオカナダモは呼吸と光合成をし、呼吸で消費される酸素の量よりも光合成で放出される酸素の量のほうが多いので、結果酸素が放出されます。そのためヒメダカの呼吸回数は増えません。
Yはオオカナダモが無いので、ヒメダカが水中の酸素が消費していき、ヒメダカの呼吸回数が増えます。
②
光の有無について問われているので、光の有無のみ異なるペットボトルWとXに着目します。
問3(2)
(答)ヒメダカの呼吸によって排出された二酸化炭素が、オオカナダモの光合成に使われるから。
光合成のメカニズムがきちんと分かっているかを問う問題です。
光合成は葉の葉緑体で行われます。
光合成とは、水と二酸化炭素を光エネルギーを利用して、酸素とデンプンを合成する反応です。
水は道管から、二酸化炭素は気孔から供給されます。
酸素は気孔から放出され、デンプンは葉緑体に貯蔵され、夜間師管を通ってからだの各部へ運ばれます。
光合成には二酸化炭素が必要なのですが、ヒメダカが呼吸をすることで供給してくれます。
光合成により酸素が多く発生するので、ヒメダカが呼吸しやすくなります。
このようにペットボトルXでは、オオカナダモとヒメダカが相互に助け合う環境が出来上がっています。
大問3 化学変化とイオン(化学分野・中3)
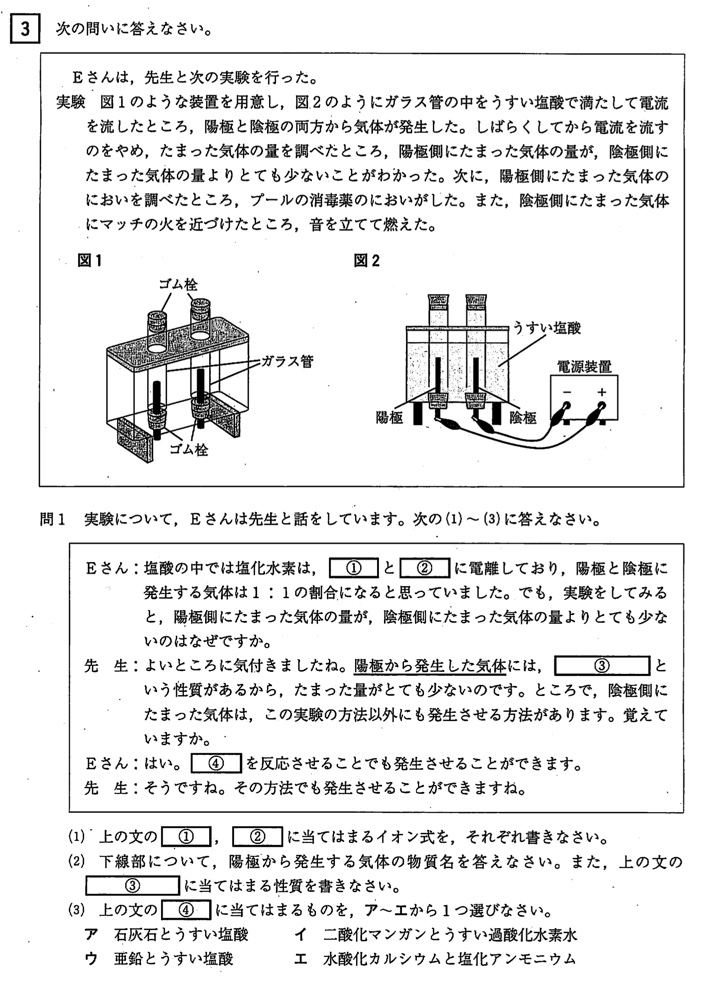
問1(1)
(答)①H+、②Cl–
塩酸の電離式は、以下のとおりです。。
HCl→H+ + Cl–
問1(2)
(答)
物質名:塩素
性質:水に溶けやすい
塩酸の電気分解は、全体の反応は以下のようになります。
2HCl → H2 + Cl2
水素(H2)と塩素(Cl2)の係数が1:1なので、体積比も1:1となり、水素と塩素が同じ体積分発生します。
しかし、陽極で塩素が発生する塩素は水に溶けやすいため、捕集できる量は塩素の方が少なくなります。
塩酸の電気分解のメカニズムですが、まず、マイナスとプラスはくっつく、ということを押さえてください。
陽極(+極)には塩化物イオン(Cl–)が、陰極(−極)には水素イオン(H+)が移動します。
陽極(+極)では塩化物イオン(Cl–)が電子を2個放出し塩素(Cl2)が、陰極(−極)では移動してきた電子を水素イオン(H+)が受け取り水素(H2)が発生します。
発生した気体の確認法として、陽極付近の水溶液に赤インクを加えると、塩素の漂白作用で赤色が脱色します。
問1(3)
(答)ウ
単なる知識問題です。
陰極から発生する気体は水素(H2)です。
水素が発生する反応として、亜鉛またはマグネシウムにうすい塩酸を加える反応があります。
選択肢アは二酸化炭素(CO2)が、選択肢イは酸素(O2)が、選択肢エはアンモニア(NH3)が発生します。
それぞれの気体について、代表的な反応式を実験方法も合わせて押さえてください。
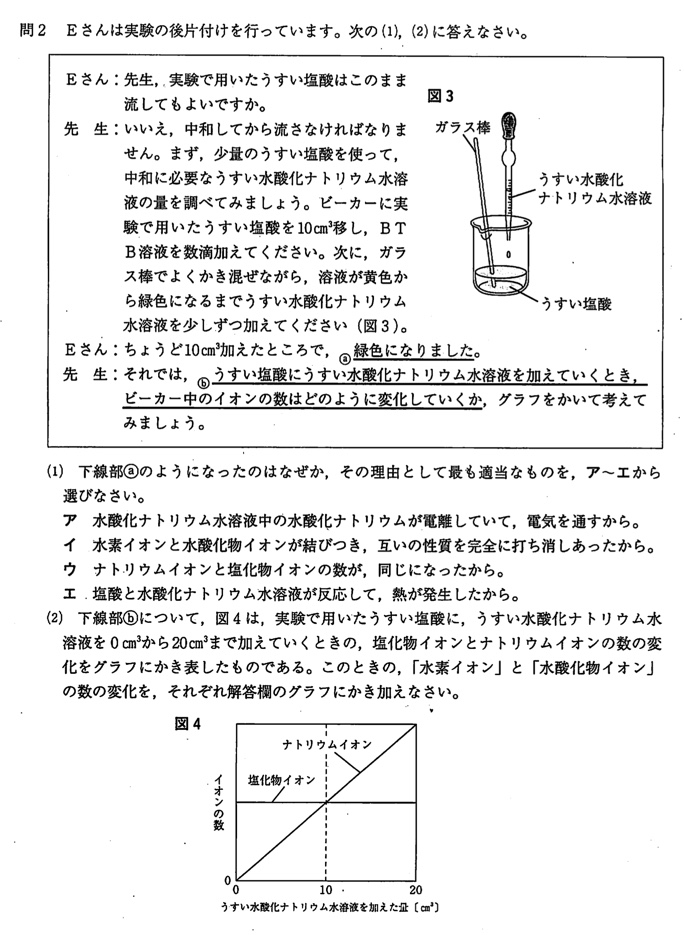
問2(1)
(答)イ
BTB溶液が黄色(酸性)→緑色(中性)になったのは、水酸化ナトリウム(NaOH)を加えることで、OH–と塩酸(HCl)のH+が結びつき、水になったからです。
選択肢エですが、中和が起こる(この場合、酸性→中性の段階)と熱が発生します。これを中和熱といいます。
中和熱は中和反応で結びつくH+とOH–の数に比例するので、中性になる量(中和点)で中和熱が最大になります。
問2(2)
水素イオン(H+)について。
うすい水酸化ナトリウム水溶液が10cm3で中和するので、H+の数は10cm3以降ゼロになります。
また、0cm3のとき塩化物イオン(Cl–)と同数になります。
塩酸(HCl )の電離式において、H+とCl–の係数比が1:1だからです。
あとは、0cm3のときとの10cm3ときの2点を結んで完成です。
0〜10cm3の範囲ですが、OH–を1個加えるとH+が1個減りますが、水酸化ナトリウム(NaOH)の電離式において、Na+とOH–の係数比が1:1なので、Na+が1個増えるとH+が1個減ります。
つまり、Na+のグラフの傾きに−を付けたのがH+のグラフの傾きになるので、Na+のグラフとH+のグラフは垂直に交わります。
水酸化物イオン(OH–)について。
うすい水酸化ナトリウム水溶液が10cm3で中和するので、OH–の数は10cm3以降から増えていきます。
水酸化ナトリウム(NaOH)の電離式において、Na+とOH–の係数比が1:1なので、Na+が1個増えるとOH–が1個増えます。
つまり、Na+のグラフの傾きとOH–のグラフの傾きが等しくなります。
大問4 天気とその変化(地学分野・中2)

問1
(答)①ア、②イ
教科書に書かれている内容です。
問題集だけでなく、教科書も必ず2〜3読してください。
問2
(答)①露点、②ア
①
単なる知識問題です。
②
部屋の気温(飽和水蒸気量)と露点(水蒸気量)の差が小さいということは、水蒸気量が多いということです。
飽和水蒸気量に占める水蒸気量が多いので、湿度は高くなります。
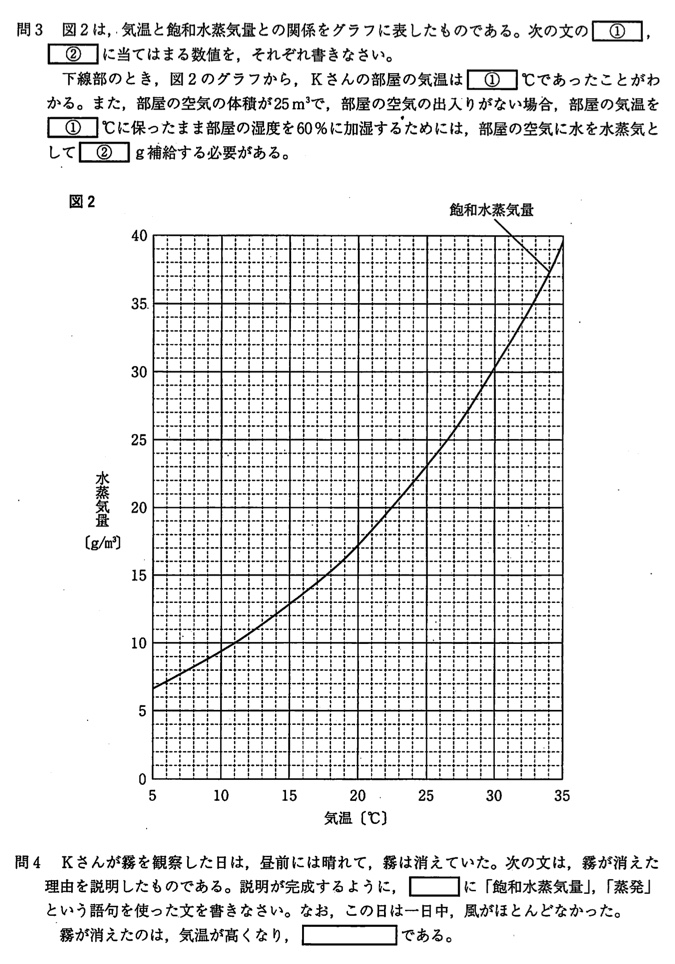
問3
(答)①26.5℃、②125g
①
露点が11℃・湿度40%という情報を元に、飽和水蒸気量を求めます。
露点が11℃のときの飽和水蒸気量は図2より、10g/m3です。
以上の情報を、湿度の公式に入れて飽和水蒸気量を求めます。
湿度(%)=露点における飽和水蒸気量(g/m3)/飽和水蒸気量(g/m3)×100
飽和水蒸気量(g/m3)=露点における飽和水蒸気量(g/m3)/湿度(%)×100=10/40×100g/m3=1/4×100g/m3=25g/m3
飽和水蒸気量が25g/m3のときの気温は図2より、26.5℃と分かります。
②
①より、部屋の気温が26.5℃のときの飽和水蒸気量は25g/m3です。
湿度が60%なので、湿度の公式より水蒸気量(g/m3)が分かります。
湿度(%)=水蒸気量(g/m3)/飽和水蒸気量(g/m3)×100
水蒸気量(g/m3)=(湿度(%)×飽和水蒸気量(g/m3))/100=(60×25)/100g/m3=60×1/4g/m3=15g/m3
水蒸気量10g/m3から15g/m3に増えているので、補給した水蒸気量は1m3あたり5g/m3です。
5g/m3に25m3をかけると、補給した水蒸気量は125gになります。
問4
(答)飽和水蒸気量が大きくなって水滴が水蒸気となったため
霧は、夜間の放射冷却で、地面付近の空気が露点に達し、水蒸気が水滴になって早朝に発生します。
早朝発生した霧は、日中気温が上がり飽和水蒸気量が大きくなって露点よりも高くなると、水滴が水蒸気となって空気中にもどります。
大問5 身のまわりの現象(物理分野・中1)

問1
(答)振幅が小さくなるため
弦の音の大小は振幅で、音の高低は振動数で表します。
なお、弦を弾いたあと音の大きさは時間とともに小さくなりますが、音の高さは一定で変わりません。
つまり、振動数は変わらず、振幅のみ小さくなっていきます。
問2
(答)イ
音の大小は弦を弾く強さで、音の高低は弦の長さで決まります。
弦を強く弾いても音が大きく(振幅が大きく)なるだけで、音の高低(振動数)は変わりません。
問3
(答)ア
弦の張りを強くしたら、振動数が多くなります。
振動数が多くなるということは波長が短くなるということなので、図2のおんさAより波の山と山との間隔が狭い選択肢アが正解です。
問4
(答)入射角:30°、屈折角:50°
以下の図を参照。
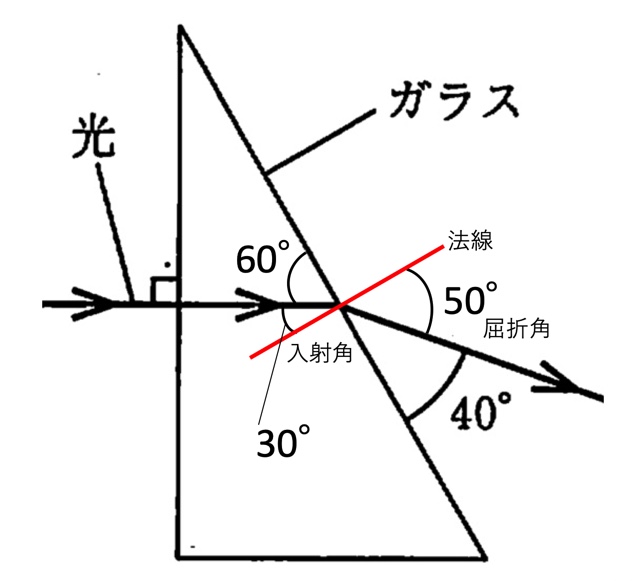
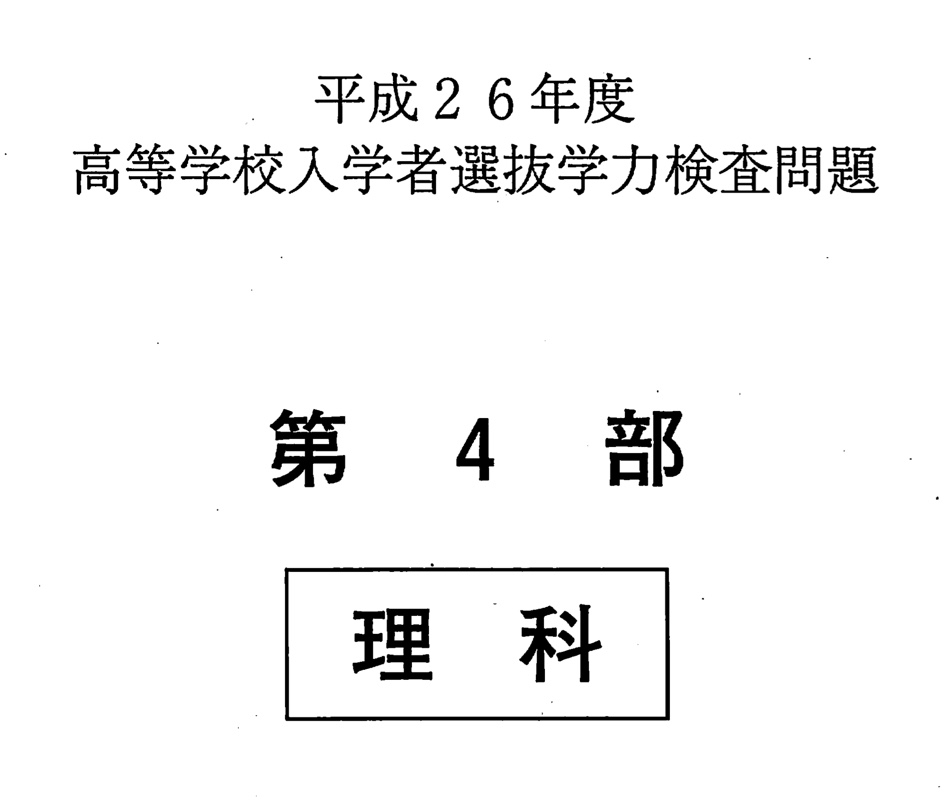
問4
(答)エ
まず、全反射について押さえましょう。
水→空気のとき、入射角49°以上で全反射します。
水→ガラスのとき、入射角42°以上で全反射します。
このときの入射角を臨界角といいます。
選択肢ア〜ウの光は、ガラスに垂直に入射したあと入射角30°で入射するので、全反射せず屈折してガラスから出ていきます。
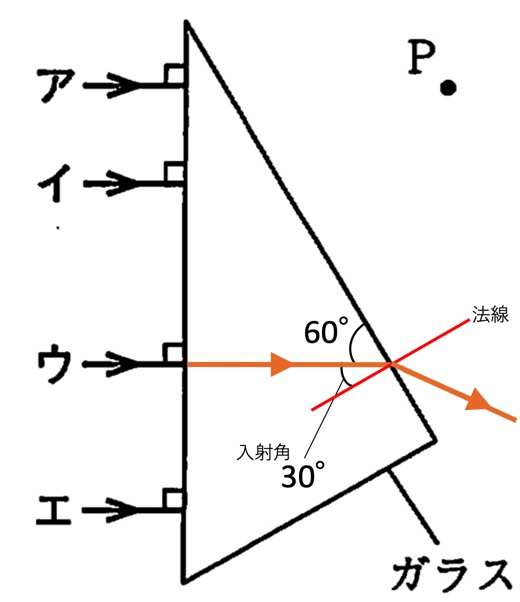
対して選択肢エの光は、ガラスに垂直に入射したあと入射角60°と、ガラス→空気の臨界角42°以上なので、全反射します。
その後入射角30°で入射するので、ガラスから屈折して出てP点を通過します。