
👉教師紹介・料金
※授業料1回1,500円+交通費(コミコミ最大3,000円)・入会金なし・お好きな日時に受講・3回のお試し期間あり(無料教材あり)
■総合ABC範囲表
>>【最新版】総合ABC範囲表
■総合A過去問
科目別:国語、数学、社会、理科、英語
年度別:2024年、2023年、2022年、2021年、2020年、2019年、2018年、2017年、2016年
■総合B過去問
科目別:国語、数学、社会、理科、英語
年度別:2024年、2023年、2022年、2021年、2020年、2019年、2018年、2017年、2016年、2015年
■総合C過去問
科目別:国語、数学、社会、理科、英語
年度別:2024年、2023年、2022年、2021年、2020年、2019年、2018年、2017年、2016年、2015年
■総合ABC道コン偏差値
>>総合ABC道コン偏差値(SS)推移
☆過去問ダウンロードはこちら☆
※生徒以外で過去問のみをお求めの方は、こちらにご連絡ください(過去問の「原本」を頂ける方は歓迎します!)。
👉お問い合わせ
中学3年北海道学力テスト総合A「理科」(2020)の難易度
私が実際に問題を見た感想ですが、過去の総合ABCの中では、最高レベルのセットだと感じました。
それでも、3月の公立高校入試問題と比較したら、かなり易しいです。
入試のゴールである『塾技 理科80』をある程度読んだ子なら、満点が取れたでしょう。
中学3年北海道学力テスト総合A「理科」(2020)の平均点・偏差値
道コンによると、2020年の総合A「理科」の平均点と偏差値は以下の通りです。
<総合A「理科」の平均点と偏差値>
34点(57点)
※道コンSS50に相当
※()内は100点満点で換算した点数
中上位公立高校を受験するなら、第5回・6回の道コンは必ず受けましょう。
>>★的中率75%★道コン中3第5回・6回の理科の信憑性は高い!高校入試で的中した証拠【画像】
中学3年北海道学力テスト総合A「理科」(2020)問題・解答・解説
大問1 身のまわりの物質(中1・化学)
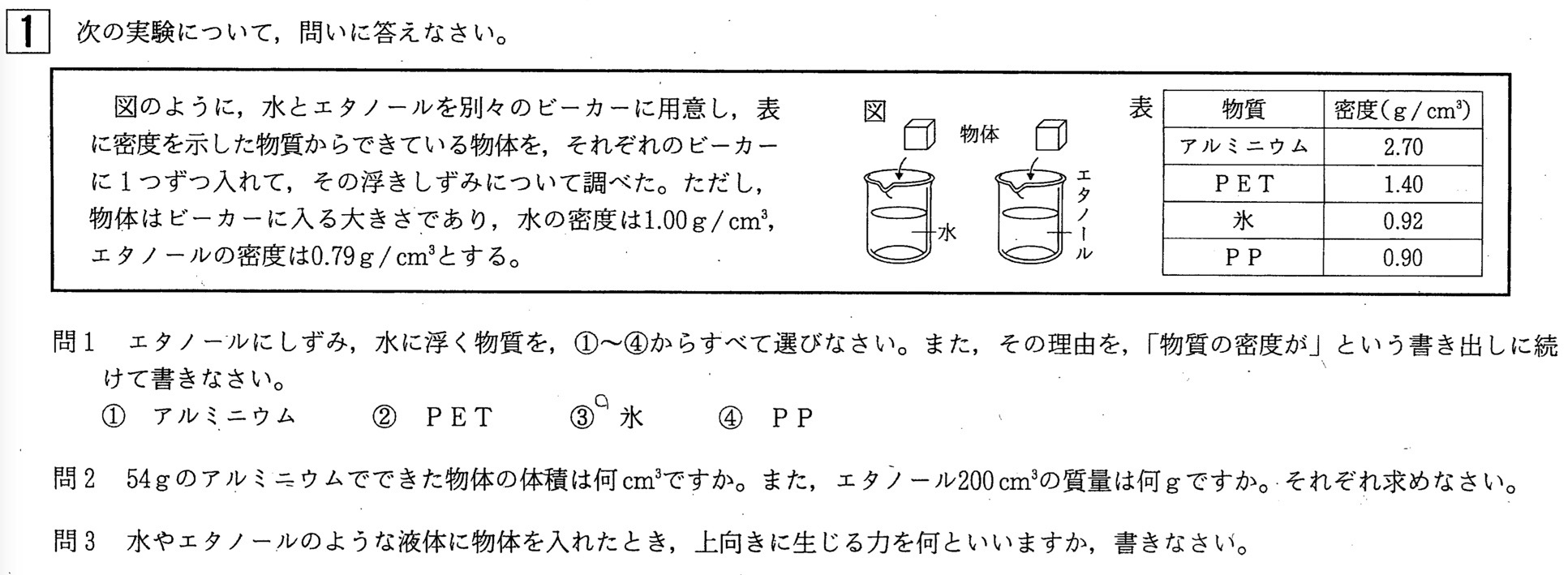
問1
解答:物質・・・③、④(順不同) 理由・・・(物質の密度が)エタノールの密度より大きく、水の密度より小さいから(例)
解説:
「浮くか沈むか」ときたら密度の大小比較をします。
密度(比重)が大きいほうが沈み、小さい方が浮きます。
密度の単位はg/cm3で、質量(g)に比例し体積(cm3)に反比例します。
例えば同一質量(g)のロウにおいて、固体のロウは液体のロウよりも体積(cm3)が少ないので、液体のロウよりも密度(g/cm3)が大きいです。
ゆえに、固体のロウは液体のロウに沈みます。
一般的に、同一質量の物質において、固体は液体よりも密度(g/cm3)が大きく、液体に沈みます。
ただし水だけは例外で、4℃のとき体積(cm3)が最小となり、密度(g/cm3)が最大となるので、氷は水に浮きます。
水たまりの水が表面から氷るのは、温度が4℃より小さい水は密度が小さいので浮き、凝固点(0℃)に達して氷るからです。
なお、固体の密度(g/cm3)と液体の密度(g/cm3)が等しいとき、固体は液体中で静止します。
物質は有機物と無機物に大別され、無機物はさらに、金属と非金属に分類されます。
プラスチックの原料は、ほとんどが石油(ナフサ)です。
石油は有機物であるので炭素(C)と水素(H)を含んでおり、燃やす(酸素O2と化合する)と二酸化炭素(CO2)と水(H2O)が発生します。
プラスチックの性質として、以下の4つがあります。
①軽くてしなやか
②熱や油、薬品に強い
③耐水性、可塑性(変形した物体が元の形に戻らない性質)にすぐれている
④生分解性プラスチックは、土のなかで微生物により分解される
プラスチックの種類として、以下の5種類を押さえておきましょう。
・ポリエチレンテレフタレート(PET):燃えにくいが多少のすすがでる
・ポリエチレン(PE):溶けながらよく燃える、水に浮く
・ポリスチレン(PS):すすを出しながら燃える
・ポリプロピレン(PP):溶けながらよく燃える、水に浮く
・ポリ塩化ビニル(PVC):燃えにくい
ポリエチレン(PE)とポリプロピレン(PP)以外は、4℃の水(密度 1.0g/cm3)より密度が大きいため、水に沈みます。
金属には、すべての金属に共通する3つの性質があります。
①みがくと光る(金属光沢)
②たたくとのびたり、広がったりする(延性・展性)
③電気や熱を通す(電気伝導性・熱伝導性)
すべての金属に共通しない性質として、「磁石につく」があります。
磁石につくのは、鉄・ニッケル・コバルトです。
以上の知識を元に、問題を解きます。
エタノールに沈み水に浮く物質(固体)なので、エタノールの密度(0.79g/cm3)より大きく水の密度(1.00g/cm3(4℃の水))より小さい物質を、表から選びます。
不等式を用いると、0.79g/cm3<x<1.00g/cm3を満たす物質なので、氷(③)とPP(④)が該当します。
問2
解答:アルミニウム・・・20(cm3)、エタノール・・・158(g)
解説:
単位計算の問題です。
まず問われているのは、アルミニウムの体積(cm3)です。
これを、アルミニウムの密度(2.70g/cm3)を軸にして算出します。
アルミニウムの質量が54gと仮定しているので、アルミニウムの体積(cm3)は、
アルミニウムの体積(cm3)=54g÷2.70g/cm3=54×10/27=2×10=20cm3
となります。
問題文に「また」とあるので、話が変わってもう一つ答える必要があります。
次に問われているのは、エタノールの質量(g)です。
これを、エタノールの密度(0.79g/cm3)を軸にして算出します。
エタノールの体積が200cm3と仮定しているので、エタノールの質量(g)は、
エタノールの質量(g)=0.79g/cm3×200cm3=79×2=158g
となります。
速度の計算でも、同じようにして計算します。
問3
解答:浮力
解説:
ばねばかりを用いて、物体の重さを水中ではかると、物体は水から鉛直上向きの力を受け、空気中ではかるよりも軽くなります。
この力を浮力といいます。
物体は水中では、上面と下面、左右の面それぞれから水の圧力である水圧を受けます。
水圧は物体が深く沈むほど、大きくなります。
左右の面が受ける水圧の大きさは等しいので、互いに打ち消し合います。
しかし、上面と下面では、下面にかかる水圧の大きさ(鉛直上向き)が上面にかかる水圧の大きさ(鉛直下向き)より大きいため、その差が浮力となります。
浮力[N]とは物体が押しのけた流体の重さ[N]ということができ、これをアルキメデスの原理といいます。
仮に、水の密度を1.0g/cm3(4℃の水)とします。
物体の体積が50cm3のとき、この物体を水に完全に沈めた場合、物体が押しのけた水の体積は50cm3、50cm3の水の質量[g]は、1.0g/cm3×50cm3=50gです。
100gの物体にはたらく重力の大きさを1Nと仮定すると、50cm3の水の重さ[N]は、1N/100g×50g=1/2N=0.5Nとなるので、物体に働く浮力の大きさは0.5Nとなります。
アルキメデスの原理より、物体に働く浮力の大きさは、物体の体積と液体の密度に依存します。
ゆえに、物体が水中に完全に沈むと、物体に働く浮力の大きさはそれ以上増加しません。
大問2 身のまわりの現象(中1・物理)

問1
解答:73(cm〜)152(cm)
解説:
太陽や豆電球など自ら光を出すものを光源といいます。
光源が見えるのは、光源からの光が直接目に入るからで、光源以外のものが見えるのは、光源から出た光が物の表面で反射し、その光が目に入るからです。
光は、さえぎるものがなければ同じ物質(空気やガラスなど)の中をまっすぐに進みます。これを光の直進といいます。
直進した光が、鏡などの面に当たって反射するとき、入射角=反射角が成り立ちます。
これを反射の法則といいます。
鏡などの面に垂直な線のことを法線といいます。
入射角、反射角、屈折角は、法線とのなす角度です。
鏡やスクリーンなどに物体がうつって見えるものを、その物体の像といいます。
鏡の像は、鏡面について物体と線対称の位置にでき、実際にそこにはない像(虚像)を見ていることになります。
鏡に反射する光の経路の作図の手順は、以下の3ステップです。
①鏡面に対して光源(物)と対称な点(像)をとる。
②像と目を直線で結び、鏡面との交点をとる。
③光源と手順②でとった点を結ぶ。
鏡にうつした物が見える範囲の作図には、以下の2通りの方法があります。
①鏡面について物体と線対称の位置に像を作図し、像と鏡の両端を通る2つの直線を作図する。
→2つの直線に挟まれた部分にいる人は、鏡にうつした物を見ることができる
②光源から鏡の両端に入射光線を引き、反射の法則から反射光線を作図する。
→反射光線に挟まれた部分にいる人は、鏡にうつした物を見ることができる
全身を鏡で見るための鏡の長さと位置は、鏡に反射する光の経路の作図手順より、以下のように導くことができます。
①鏡の上端の位置:目から上において、頭上から目の高さ×1/2
②鏡の下端の位置:目から下において、つま先から目の高さ×1/2
③必要な鏡の長さ:身長×1/2
以上の知識を元に、問題を解きます。
問われているのは、全身を写すための鏡の上端と下端の床からの距離であることに注意して解きます。
図より、Aさんのつま先から目の高さは146cmなので、鏡の下端の位置は146cm×1/2=73cmです。
Aさんの頭上から目の高さは12cm(158cm – 146cm)なので、鏡の上端の位置は146cm+12cm×1/2=146+6=152cmです。
以上より、全身を写すための鏡の上端と下端の床からの距離は、73cm〜152cmとなります。
問2
解答:1mの距離・・・ウ、4mの距離・・・ウ
解説:
鏡で全身を見るのに必要な要素は、鏡の上下の長さが身長の1/2であることだけで、鏡からの距離と見える範囲は相関しません。
鏡に反射する光の経路の作図の手順は、以下の3ステップです。
①鏡面に対して光源(物)と対称な点(像)をとる。
②像と目を直線で結び、鏡面との交点をとる。
③光源と手順②でとった点を結ぶ。
上記の作図手順により二等辺三角形ができますが、人と鏡との距離により頂角は変化するが、底辺の長さが変わらないため、鏡の上端と下端の位置は変わらず、鏡からの距離と見える範囲は相関しません。
問3
解答:①・・・入射角、②・・・反射角(順不同)
解説:
問1解説参照。
大問3 身のまわりの現象(中1・物理)

問1
解答:イ
解説:
おんさやモノコードの弦などを音源といいます。
おんさを叩いたり、モノコードを弾くなどすると、音源が振動し、その振動が波として広がり、空気などの音を伝える物質(媒質)に次々と伝わることで、音が伝わります。
このようにして広がる音の波を音波といいます。
空気の成分比率は、体積の割合で多い順から
窒素(約78%)、酸素(約21%)、アルゴン(約0.9%)、二酸化炭素(約0.04%)です。
このほか、ネオン、ヘリウムなども微量ですが含まれています。
これら空気を構成する原子や分子は質量[g]を持つ物体で、音波によって振動し、その振動が伝わっていくことで、音が伝わります。
同様に、水には水分子が、金属には銅原子や鉄原子などがあり、それらに音波の振動が伝わっていくことで、音が伝わります。
なお、音を伝える物質と音が伝わる速さは、気体<液体<固体の順に速くなります。
例えば、空気中での音が伝わる速さは約340m/s、水中での音が伝わる速さは約1500m/s、鉄の場合は約6000m/s、です。
音源が1回振動すると、音源のまわりの空気が押されたり引かれたりして密度が変化し、1組の山と谷ができます。
コンピューターを用いて波形を調べると、図1のような波形になります。
このとき、中央を横切る線であるベースラインから、山または谷までの幅を振幅といいます。
振幅が大きいほど音が大きく、振幅が小さいほど音が小さいです。
音波の波形は、左から右に動いています。
1つの波が通過すると1回振動したといいます。
振動数とは、1秒間あたりに通過する波の数で、単位はHz(ヘルツ)です。
振動数が多いほど音が高く、振動数が小さいほど音が低いです。
以上の知識をもとに、問題を解きます。
①の図で、音の振幅(音の大きさ)を表すのはイ、音の振動数(音の高低)を表すのはウです。
ウは一つの波で、エはその半分で半波長といいます。
問2
解答:400(Hz)
解説:
振動数とは、1秒間あたりに通過する波の数で、単位はHz(ヘルツ)です。
1つの波が通過するとは1回振動したということです。
本問では、0.01秒で4回振動したことから、振動数は、
振動数(Hz)=4/0.01s=400Hz
問3
解答:振幅・・・大きさ、振動数・・・高さ
解説:
問1解説参照。
問4
解答:1190(m)
解説:
単位計算の問題です。
問われているのは距離(m)で、これを速さの単位(m/s)を用いて算出します。
ここで欲しいのは秒(s)で、分かっているのは1秒間に30コマつまり30コマ/sと、105コマなので、
秒(s)=105コマ÷30コマ/s=105/30s=35/10s=3.5s
以上より距離(m)は、
距離(m)=340m/s×3.5s=340×(3+0.5)=1020+170=1190m
大問4 電流とその利用(中2・物理)

問1
解答:10(Ω)
解説:
回路とは、電流が電源装置の+極から出て−極にもどるひと回りの道のことです。
抵抗に電圧を加えると電流が流れます。
電圧→電流、という流れです。
抵抗とは、電流の流れにくさを表します。
金属線は抵抗が小さい材料で、このまま電圧を加えると、回路に大きな電流が流れてしまい危険です。
そこで、抵抗が大きい抵抗器や電熱線や豆電球などを接続して、回路に大きな電流が流れないようにします。
電流は+の電気で、電源装置の+極から出て、-極に戻るかたちで回路を流れます。
回路に流れる電流の大きさを測定する装置を電流計、
回路に加わる電圧の大きさを測定する装置を電圧計といいます。
電流計も電圧計も、+端子は電源の+極側に、−端子はまず3つの−端子のうち最大のものにつなぎます。
測定部分に対し、電流計は直列に、電圧計は並列に接続します。
抵抗に流れる電流と電圧の関係をオームの法則といい、以下の式で表されます。
V[V]=I[A]×R[Ω]
上の式を変形して、
V[V]=I[A]×R[Ω] ⇔ I=1/R × V
抵抗は材料によって決まっている、つまり一定であるので、抵抗に流れる電流の大きさは、抵抗に加わる電圧の大きさに比例し、比例定数は1/R(抵抗の逆数)です。
以上の知識をもとに、問題を解きます。
グラフの格子点の一つ(0.1A、1V)を、オームの法則に代入します。
V[V]=I[A]×R[Ω] ⇔ R=V/I=1V/0.1A=10Ω
問2
解答:2160(J)
解説:
抵抗である電熱線に電流が流れると、電気エネルギー[J]が発生します。
電気エネルギーW[J]は、1秒間あたりに発生する電気エネルギーである消費電力P[W]=P[J/s]と、電流が流れた時間[s]の積で表されます。
W[J]=P[W]×t[s]
消費電力P[W]=P[J/s]は、以下の式で表されます。
P[W]=P[J/s]=I[A]×V[V]=I2R=V2/R
ゆえに、電気エネルギーW[J]は、以下の式で表されます。
W[J]=P[W]×t[s]=I[A]×V[V]×t[s]=I2Rt=V2t/R
エネルギーは移り変わります。
抵抗で発生した電気エネルギーW[J]は、多くの場合、熱エネルギーQ[J]として移り変わります。
熱エネルギーは、発熱量ともいいます。
発熱量Q[J]は、以下の式で表されます。
Q[J]=W[J]=P[W]×t[s]=I[A]×V[V]×t[s]=I2Rt=V2t/R
また、水温上昇と発熱量の関係、つまり水が得た熱エネルギーは、以下の式で表されます。
発熱量[J]=水が得た熱エネルギー=4.2×水の質量[g]×上昇温度[℃]
以上の知識をもとに、問題を解きます。
分かっている値は、抵抗(10Ω)、電圧(6V)なので、発熱量Q[J]の式として、
Q[J]=V2t/R
を用いて計算します。
Q[J]=(6V)2/10Ω×(10×60s)=36×60=216×10=2160J
問3(やや難)
解答:①・・・イ、②・・・ウ
解説:
水温上昇と発熱量の関係、つまり水が得た熱エネルギーは、以下の式で表されます。
発熱量[J]=水が得た熱エネルギー=4.2×水の質量[g]×上昇温度[℃]
上の式を上昇温度[℃]について解くと、
上昇温度[℃]=発熱量[J]/(4.2×水の質量[g])
上の式の発熱量[J]とは水が得た熱エネルギーで、電熱線から発生した発熱量Q[J]とは異なります。
エネルギーは様々な形で移り変わります。
電熱線から発生した電気エネルギー[J]は全て熱エネルギー(発熱量Q[J])に移り変わるのではなく、一部音エネルギーや光エネルギーに変わります。
ゆえに、水が得た熱エネルギー≠発熱量Q[J]です。
しかし問題文には「水温はおよそ何℃上昇しますか」と、概算値が問われているので、水が得た熱エネルギー=発熱量Q[J]と仮定して計算してもOKです。
これより、上昇温度[℃]は以下の式で表すことができます。
上昇温度[℃]=発熱量[J]/(4.2×水の質量[g])=発熱量Q[J]/(4.2×水の質量[g])=V2t/(R×4.2×水の質量[g])
ここまでを踏まえて、問題を解きます。
①
変化しているのは、水の質量[g]だけです。
水の質量[g]が100gから50gと、1/2倍になっています。
先の上昇温度[℃]の式で、水の質量[g]は分母にあるので、上昇温度[℃]は2倍に変化することになります。
問題文で、水の質量[g]が100gのときの上昇温度が5℃(24℃-19℃)とあるので、水の質量[g]が50gのときの上昇温度は、およそ5℃×2=10℃(イ)であると考えられます。
②
変化しているのは、電圧[V]だけです。
電圧が[V]が6Vから12Vと、2倍になっています。
先の上昇温度[℃]の式で、電圧[V]は分子にあり、電圧の2乗なので、上昇温度[℃]は22=4倍に変化することになります。
問題文で、水の質量[g]が100gのときの上昇温度が5℃(24℃-19℃)とあるので、電圧が[V]が12Vのときの上昇温度は、およそ5℃×4=20℃(ウ)であると考えられます。
大問5 電流とその利用(中2・物理)
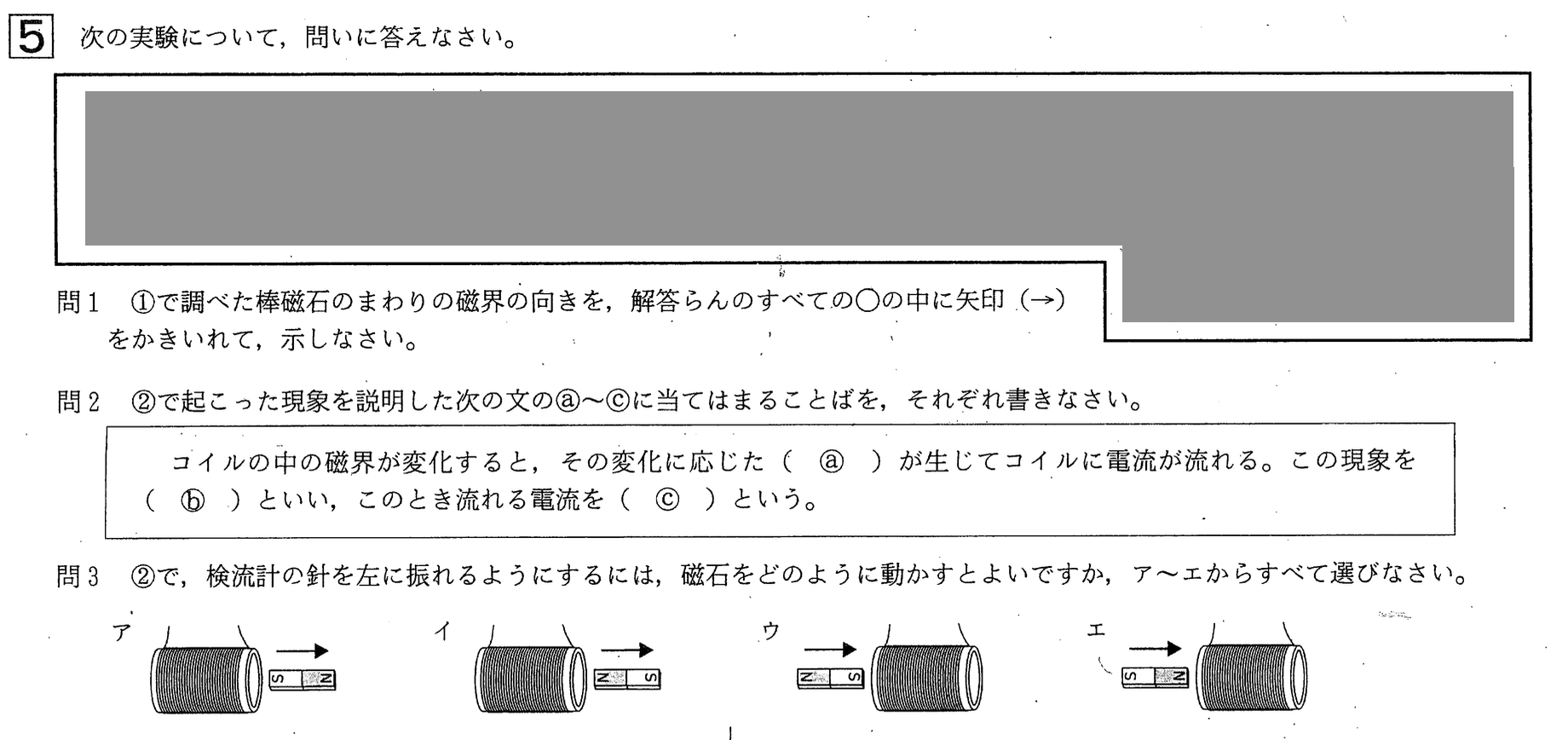
問1
解答:
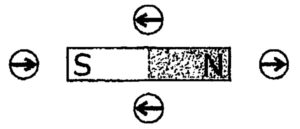
解説:
磁石では、N極からS極に磁力線が流れます。磁界の向きはN極が指し示す向きです。
N極から出るのが磁界の向き、と覚えると分かりやすいです。
以上より、解答例のとおりとなります。
問2
解答:a・・・電圧、b・・・電磁誘導、c・・・誘導電流
解説:
コイル内の磁界が変化すると、磁界の変化を打ち消すようにコイルに電圧が生じて電流が流れます。
この現象を電磁誘導、電磁誘導によって流れる電流を誘導電流といいます。
誘導電流は、以下のときに大きくなります。
①磁石を出し入れする動きを速くする
②コイルの巻き数を多くする
③コイルの内径を小さくする
問3
解答:ア、ウ(順不同)
解説:
棒磁石のN極をコイルの上端に近づけると、コイルの上端から下端に向けて、下向きの磁力線が流れます。
その磁界の変化を打ち消すように、コイルの上端がN極となって、コイルから上向きの磁力線が発生します。
また、棒磁石のS極をコイルの上端に近づけると、コイルの上端がS極となります。
その逆として、棒磁石のN極をコイルの上端から遠ざけると、コイルの上端がS極となります。
棒磁石のS極をコイルの上端から遠ざけると、コイルの上端がN極となります。
誘導電流の向きは、『塾技 理科80』の右手のグーより決定できます。
これらの法則を、レンツの法則といいます。
N極どうしS極どうしは反発するが、N極とS極はくっつく、と覚えると分かりやすいでしょう。
以上の知識を元に、問題を解きます。
図2において、レンツの法則より、コイルの右側に棒磁石のS極を近づけると、コイルの右側はS極になります。
コイルが巻かれた向きが図からは分からないので、誘導電流の向きは不明ですが、検流計の針は右側に触れたと問題文に書かれています。
本問では、検流計の針が左側に触れる場合を選択するので、図2と逆の状況すなわちコイルの右側はN極になる状況を選択すればOKです。
ア:棒磁石のS極をコイルの右側から遠ざけているので、コイルの右側はN極となるので正解です。
イ:棒磁石のN極をコイルの右側から遠ざけているので、コイルの右側はS極となるので誤りです。
ウ:棒磁石のS極をコイルの左側から近づけているので、コイルの左側はS極となり、コイルの右側はN極となるので正解です。
ウ:棒磁石のN極をコイルの左側から近づけているので、コイルの左側はN極となり、コイルの右側はS極となるので誤りです。
大問6 植物の生活と種類(中1・生物)

問1
解答:胞子のう
解説:
植物の分類の観点はまず、種子をつくるか否かで大別します。
種子を作る植物を種子植物といいます。
種子植物はさらに、胚珠が子房に包まれているか否かで分類し、胚珠が子房に包まれている植物を被子植物、胚珠がむきだしの植物を裸子植物といいます。
被子植物はさらに、子葉の枚数で分類し、子葉が1枚の植物を単子葉類、子葉が2枚の植物を双子葉類といいます。
双子葉類はさらに、花弁がくっついているか否かで分類し、花弁がくっついている植物を合弁花類(ツツジ)、花弁が離れている植物を離弁花類(アブラナ)といいます。
単子葉類として、イネ・トウモロコシ・スズメノカタビラ・ユリ・アヤメ・ツユクサ・チューリップを、
合弁花類として、ツツジ・タンポポ・アサガオを、
離弁花類として、サクラ・アブラナ・エンドウを、
裸子植物として、マツ、スギ、ヒノキ、イチョウ、ソテツを
それぞれ覚えましょう。
これに加えて、ホウセンカは双子葉類であることも覚えましょう。
双子葉類は、子葉が2枚、葉脈(葉の維管束)が網状脈、茎の維管束が輪状に並びます。
維管束とは、道管と師管の束のことです。
道管は、根から吸収された水や肥料分が通る管で、茎では維管束の内側にあります。
師管は、葉で光合成で作られた養分(デンプン→ショ糖)が通る管で、茎では維管束の外側にあります。
双子葉類の根は、主根と側根からなり、根の先端ちかくに根毛があり、表面積を広げる構造をしており、これにより水や肥料分を効率よく吸収できます。
単子葉類は、子葉が1枚、葉脈(葉の維管束)が平行脈、茎の維管束が全体に散らばっています。
双子葉類と同じく、茎では道管は維管束の内側に、師管は維管束の外側にあります。
単子葉類の根はひげ根で、根の先端ちかくに根毛があり、表面積を広げる構造をしており、これにより水や肥料分を効率よく吸収できます。
種子をつくらず、胞子で増える植物は、今度は維管束があるかどうか、または、根・茎・葉の区別かあるかどうかで大別され、
維管束がある植物をシダ植物、ない植物をコケ植物といいます。
イヌワラビはシダ植物です。
シダ植物の個体の増やし方は、
葉の裏にある胞子のうが乾いて裂けて胞子が飛び出て、胞子が発芽して前葉体となり、前葉体の造精器(雄器)から精子が雨の日に泳いで別の前葉体の造卵器(雌器)の卵までいき受精し、受精卵が成長し若いシダとなって増えます。
シダ植物は、無性生殖→有性生殖の順で個体を増やします。
スギゴケやゼニゴケはコケ植物です。
コケ植物は、雄株と雌株の区別があるものが多いです。
個体の増やし方は、
雄株の雄器で精子が、雌株の雌器で卵が作られ、雨の日などに精子が雌器の卵まで泳いで受精し、受精卵が育つと雌器に胞子のうができて胞子がつくられ、胞子のうが破れて胞子が飛び散り、発芽・成長して雄株と雌株になります。
コケ植物は、有性生殖→無性生殖の順で個体を増やします。
シダ植物の根は、種子植物ほど発達していないひげ根、
茎は、地中を横に走る地下茎、
葉は、地上に出ている部分全体が1枚の葉(複葉という)です。
シダ植物として、イヌワラビ・ゼンマイ・スギナを、
コケ植物として、スギゴケ・ゼニゴケを、
それぞれ覚えましょう。
シダ植物とコケ植物の相違点について。
シダ植物は、根・茎・葉(維管束)の区別があり根(ひげ根)で水を吸収します。
コケ植物は、根・茎・葉(維管束)の区別がなく、からだの表面で水を吸収します。また、雄株と雌株に分かれていることが多いです。仮根は水を吸収する力は弱く、主にからだを地面に固定するはたらきをします。
シダ植物とコケ植物の類似点について。
種子ではなく胞子で増える、湿ったところで生育する、葉緑体を持ち光合成をする、雄器で作られた精子が泳ぐために受精には水が必要、の4つです。
以上の知識をもとに、問題を解きます。
イヌワラビの葉の裏には、図3のように胞子のうがあります。
葉の裏にある胞子のうが乾いて裂けて胞子が飛び出て、胞子が発芽して前葉体となり、前葉体の造精器(雄器)から精子が雨の日に泳いで別の前葉体の造卵器(雌器)の卵までいき受精し、受精卵が成長し若いシダとなって増えます。
問2
解答:X・・・仮根、はたらき・・・エ
解説:
コケ植物は、根・茎・葉(維管束)の区別がなく、からだの表面で水を吸収します。また、雄株と雌株に分かれていることが多いです。
仮根は水を吸収する力は弱く、主にからだを地面に固定するはたらきをします。
問3
解答:Ⅰ・・・D・F、Ⅱ・・・A・B、Ⅲ・・・C・E(それぞれ順不同)
解説:
シダ植物とコケ植物の相違点について。
シダ植物は、根・茎・葉(維管束)の区別があり根(ひげ根)で水を吸収します。
コケ植物は、根・茎・葉(維管束)の区別がなく、からだの表面で水を吸収します。また、雄株と雌株に分かれていることが多いです。仮根は水を吸収する力は弱く、主にからだを地面に固定するはたらきをします。
シダ植物とコケ植物の類似点について。
種子ではなく胞子で増える、湿ったところで生育する、葉緑体を持ち光合成をする、雄器で作られた精子が泳ぐために受精には水が必要、の4つです。
以上の解説をもとにすると、答えが得られます。
問4
解答:a、d(順不同)
解説:
単子葉類として、イネ・トウモロコシ・スズメノカタビラ・ユリ・アヤメ・ツユクサ・チューリップを、
合弁花類として、ツツジ・タンポポ・アサガオを、
離弁花類として、サクラ・アブラナ・エンドウを、
裸子植物として、マツ、スギ、ヒノキ、イチョウ、ソテツを、
シダ植物として、イヌワラビ・ゼンマイ・スギナを、
コケ植物として、スギゴケ・ゼニゴケを、
それぞれ覚えましょう。
大問7 植物の生活と種類(中1・生物)

問1
解答:イ
解説:
植物は光合成と呼吸を同時に行います。
植物の葉には葉緑体があり、光合成は葉緑体で行われます。
根で吸収した水が茎の道管(維管束の内側)から葉の維管束である葉脈(維管束の上側)を通り葉緑体に届けられ、
孔辺細胞の隙間である気孔で吸収された二酸化炭素を日光(光エネルギー)を用いて、単糖類であるグルコース(ブドウ糖)と酸素に合成されます。
グルコースは水に溶けやすく、このままの形では葉に栄養分を貯蔵できないため、グルコースが多数つながった水に溶けにくいデンプンにつくり変えられます。
夜間に水に溶けやすい二糖類のスクロース(ショ糖)に変えられ、師管を通ってからだの各部へ運ばれて、呼吸や成長の材料として使われます。
光合成では、葉の気孔から、二酸化炭素が入り酸素が出ます。
呼吸では、葉の気孔から、酸素が入り二酸化炭素が出ます。
光の当たる場所では、光合成のはたらきの方が強くなるので、光合成で出入りする気体の量が、呼吸で出入りする気体の量より多くなり、あたかも二酸化炭素が吸収され、酸素が放出されているかのように見えます。
対して植物の呼吸は、昼夜を問わず、一日中行われます。
対照実験では、ある実験を「調べたい条件」以外のものをすべて同じにした状態で行い、両者を比べることで結果が異なれば、「調べたい条件」が原因と証明できます。
葉が呼吸をして二酸化炭素を出していることは、CとDを比べることで分かります。
また、AとBを比較することで、植物が光合成をしていることが分かります。
石灰水を変化させた、すなわち石灰水を白く濁らせた植物のはたらきは、植物の呼吸です。
なお、石灰水とは水酸化カルシウム(Ca(OH)2)のことです。
水酸化カルシウムは水溶液中に水酸化物イオン(OH–)があるので、アルカリ性です。
水酸化カルシウム水溶液に二酸化炭素(CO2)が溶けると炭酸(H2CO3)となり、水素イオン(H+)が放出されるので、酸性の性質を示します。
アルカリ性の水酸化カルシウムに、酸性の炭酸が加わることで中和が起こり、炭酸カルシウム(CaCO3)の塩が発生します。
炭酸カルシウムは白色の固体で、水にとけにくいため、水溶液中に拡散します。
石灰水が白く濁るのは、炭酸カルシウムが水溶液中に拡散しているためです。
この状態でさらに二酸化炭素を流すと、炭酸カルシウムは水に溶けやすい炭酸水素カルシウムとなり、水溶液は再び透明になります。
問2
解答:名前・・・二酸化炭素、化学式・・・CO2
解説:
石灰水を変化させた、すなわち石灰水を白く濁らせた植物のはたらきは、植物の呼吸です。
呼吸では、葉の気孔から、酸素が入り二酸化炭素(化学式:CO2)が出ます。
問3
解答:(問2の気体が、)光合成によって使われたから(例)
解説:
光合成では、葉の気孔から、二酸化炭素が入り酸素が出ます。
呼吸では、葉の気孔から、酸素が入り二酸化炭素が出ます。
光の当たる場所では、光合成のはたらきの方が強くなるので、光合成で出入りする気体の量が、呼吸で出入りする気体の量より多くなり、あたかも二酸化炭素が吸収され、酸素が放出されているかのように見えます。
問4
解答:対照(実験)
解説:
対照実験では、ある実験を「調べたい条件」以外のものをすべて同じにした状態で行い、両者を比べることで結果が異なれば、「調べたい条件」が原因と証明できます。
葉が呼吸をして二酸化炭素を出していることは、CとDを比べることで分かります。
また、AとBを比較することで、植物が光合成をしていることが分かります。
大問8 動物の生活と生物の変遷(中2・生物)

問1
解答:染色液・・・酢酸オルセイン(溶液)、酢酸カーミン(溶液)、酢酸ダーリア(溶液)など 染まったつくり・・・核
解説:
生命の基本単位は、細胞です。
細胞は、核と細胞質からなる原形質と、原形質以外の後形質とからなります。
核は、中に遺伝子をのせた染色体を持ちます。
染色体は、遺伝子の本体として働く物質であるDNAと、ヒストンというタンパク質からなる糸状の構造物で、染色液によく染まることから、染色体と名が付けられています。
(染色体の”染色”の名の由来)
染色液として、以下の3種類を覚えましょう。
・酢酸カーミン溶液(赤色に染まる)
・酢酸オルセイン溶液(赤紫色に染まる)
・酢酸ダーリア溶液(青紫色に染まる)
細胞の細胞質の中には、核、細胞膜、葉緑体、液胞、ミトコンドリア、ゴルジ体、中心体などがあります。
・細胞膜:細胞内外を区切るとともに、物質の出入りを調節します。
・葉緑体:葉緑素(クロロフィル)を含み、光合成を行います。
・液胞:細胞中の水分量の調節や糖・無機塩類・不要物などを蓄積します。
・ミトコンドリア:細胞呼吸が行われる場所です。細胞は、生命活動に必要なエネルギーを得るために、ブドウ糖などの有機物を酸素を用いて分解する、呼吸を行っています。この細胞の呼吸を、肺などの呼吸器での呼吸(外呼吸)に対して、内呼吸といいます。
・ゴルジ体:おもに動物細胞にあり、細胞の分泌活動(物質を生産し、細胞外に出す働き)に関係しています。ゴルジ体は、とくに消化腺で発達しています。
・中心体:おもに動物細胞の核の近くにあり、動物細胞が体細胞分裂・減数分裂するときに出る、紡錘体形成の中心として働きます。
細胞の後形質は、細胞壁です。細胞壁は、細胞内の保護と形の保持を行っています。
動物細胞には、核・核小体・細胞質・細胞膜・ミトコンドリア・ゴルジ体・中心体などがあります。
植物細胞には、核・核小体・細胞質・細胞膜・葉緑体・ミトコンドリア・液胞・細胞壁などがあります。
問2(ややこしい)
解答:細胞壁
解説:
図1の植物細胞では、核・細胞質・葉緑体・細胞膜・細胞壁が作図されていることが分かります。
図2の動物細胞では、核・細胞質・細胞膜が作図されていることが分かります。
図1にある葉緑体と細胞壁は、図2にはありません。
問われているのは、図1にあって図2に無い葉緑体以外のものなので、細胞壁が答えです。
問3
解答:①・・・組織、②・・・器官
解説:
多くの細胞が集まり、1つのからだをつくっている生物を、多細胞生物といいます。
多細胞生物では、形やはたらきが同じ細胞が集まり組織を、組織が集まり器官を、器官が集まり個体をつくっています。
細胞→組織→器官→個体、の順で生物は形づくられています。
植物の組織の例として道管・師管が、植物の器官として、根・茎・葉・花などがあります。
動物の組織の例として上皮・神経・筋組織が、動物の器官として、皮膚・目・心臓・胃などがあります。
問4
解答: 生物・・・多細胞生物 なかま・・・a
解説:
水中の生物で、遊泳能力がないか、あっても弱いため水中を浮遊するものをプランクトンといいます。
プランクトンには、光合成を行う植物プランクトン、摂食を行う動物プランクトン、光合成も摂食も行うプランクトンがあり、
さらに、からだのつくりにより、単細胞生物と多細胞生物に分けられます。
プランクトンの例として、以下のものを覚えましょう。
植物プランクトン・多細胞生物→アオミドロ
植物プランクトン・単細胞生物→ミカヅキモ(d)、ケイソウ、ミドリムシ
動物プランクトン・多細胞生物→ミジンコ(a)
動物プランクトン・単細胞生物→ミドリムシ、アメーバ(c)、ゾウリムシ(b)
このうち、ミドリムシはべん毛、ゾウリムシは繊毛、アメーバは仮足、ミジンコは触角を使って動きますが、ミカヅキモは生きているときには自らはほとんど動きません。
ゾウリムシは動物プランクトンより、動物細胞とおなじつくりをしていると考えてよいです。
大問9 天気とその変化(中2・地学)

問1
解答:a・・・ア、b・・・イ
解説:
気体の水を水蒸気といいます。
湯気(水蒸気が冷えてできた水の粒)は見えますが、水蒸気は見えません。
空気は水蒸気を含むことができる入れ物とみなせます。
空気が水蒸気をどのくらい含むことができるのかを表す尺度として、1辺が1m・体積1m3の立方体の空気中に含まれている水蒸気量(g)、単位[g/m3]を用います。
空気に含まれる水蒸気が最大になっている状態を、水蒸気で飽和しているといい、空気1m3が含むことができる最大の水蒸気量を、飽和水蒸気量といいます。
ある量の水蒸気を含む空気の温度を下げていくと、含みきれなくなった水蒸気量が凝結して水滴となって現れます。このときの温度を露点といいます。
空気は温度が上がると、水蒸気をより多く含むことができます。
温度と飽和水蒸気量の関係を表したグラフが、飽和水蒸気量曲線です。
ある温度の空気において、飽和水蒸気量に対する含まれている水蒸気量の割合を湿度といいます。
湿度は、以下の式で表すことができます。
・湿度(%)=水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100
ある量の水蒸気を含む空気の温度を下げていくと、含みきれなくなった水蒸気量が凝結して水滴となって現れます。このときの温度を露点といいます。
つまり、ある空気が含む水蒸気量はその空気の露点における飽和水蒸気量となるので、湿度の式は、以下の式で表すことができます。
・湿度(%)=水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100=露点における飽和水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100
ある空気が含む水蒸気量は、その空気の露点における飽和水蒸気量です。
つまり、露点が高いと水蒸気量が多くなり、湿度が高くなり、露点が低いと水蒸気量が少なくなり、湿度が低くなります。
このように、露点は、空気中に含まれる水蒸気によってのみ決まります。
地面が太陽熱などで暖められると上昇気流が生じて、空気は上昇します。
空気は上昇すると膨張して温度が下がります。
空気の成分比率は、体積の割合で多い順から、窒素(約78%)、酸素(約21%)、アルゴン(約0.9%)、二酸化炭素(約0.04%)です。このほか、ネオン、ヘリウムなども微量ですが含まれています。
これらの気体分子(粒子)は、上空の空気による大気圧により押されていますが、空気が上昇すると大気圧が低くなって空気の圧力のほうが高くなるため、膨張します。
膨張するとは、空気の粒子の動きが盛んになる、つまり空気の粒子の運動エネルギー[J]が大きくなるということです。
エネルギーは移り変わります。
空気の粒子の運動エネルギー[J]は、その空気がもつ熱エネルギー[J]によってのみまかなわれ、膨張の際の外部との熱の出入りがありません。
これを断熱膨張といいます。
空気が断熱膨張すると、熱エネルギーが失われるので、空気の温度が下がっていきます。
こうして、空気の温度が露点以下となって、含みきれなくなった水蒸気量が凝結して水滴となって現れます。
さらに空気が上昇して温度が下がると、氷の結晶ができはじめます。
雲は、小さな水滴や氷の結晶が集まってできたものです。
上昇気流によって支えられているため粒は落下しませんが、粒どうしが衝突し合うなどして大きく成長すると落下し、雨や雪が降ります。
雲の発生実験として、丸底フラスコに線香のけむりとぬるま湯を入れて、ピストンを引く実験があります。
ピストンを引くと、丸底フラスコ内の空気の気圧が下がるので、丸底フラスコ内の空気が断熱膨張し、温度が下がり、露点以下となって容器内が線香の煙が水滴をつくる核となって、白く曇ります。
実験の際に、丸底フラスコ内にぬるま湯を入れるのは、水蒸気量を増やして、湿度を100%近くまで高め、温度がわずかに下がっただけで露点に達して水滴が発生するようにするためです。
以上の知識を元に、問題を解きます。
・湿度(%)=水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100
ビーカー内の空気が氷によって冷やされると、飽和水蒸気量[g/m3]が下がります。
水蒸気量[g/m3]が変化していないので、分母の飽和水蒸気量[g/m3]が小さくなると、全体の値である湿度(%)は大きくなります。
ある量の水蒸気を含む空気の温度を下げていくと、含みきれなくなった水蒸気量が凝結して水滴となって現れます。このときの温度を露点といいます。
問2
解答:55(%)
解説:
コップの温度がくもり始めた温度12℃は、露点です。
・湿度(%)=水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100=露点における飽和水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100
露点における飽和水蒸気量[g/m3]=10.7g/m3
飽和水蒸気量[g/m3]=19.4g/m3
より、
湿度(%)=10.7g/m3/19.4g/m3×100≒0.551×100=55.1≒55%
問3(やや難)
解答:空気中にふくまれている水蒸気の量に違いがあったから。(例)
解説:
空気は水蒸気を含むことができる入れ物とみなせます。
空気が水蒸気をどのくらい含むことができるのかを表す尺度として、1辺が1m・体積1m3の立方体の空気中に含まれている水蒸気量(g)、単位[g/m3]を用います。
空気に含まれる水蒸気が最大になっている状態を、水蒸気で飽和しているといい、空気1m3が含むことができる最大の水蒸気量を、飽和水蒸気量といいます。
ある量の水蒸気を含む空気の温度を下げていくと、含みきれなくなった水蒸気量が凝結して水滴となって現れます。このときの温度を露点といいます。
空気は温度が上がると、水蒸気をより多く含むことができます。
・湿度(%)=水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100=露点における飽和水蒸気量[g/m3]/飽和水蒸気量[g/m3]×100
ある空気が含む水蒸気量は、その空気の露点における飽和水蒸気量です。
つまり、露点が高いと水蒸気量が多くなり、湿度が高くなり、露点が低いと水蒸気量が少なくなり、湿度が低くなります。
このように、露点は、空気中に含まれる水蒸気によってのみ決まります。
温度と飽和水蒸気量の関係を表したグラフが、飽和水蒸気量曲線です。
以上の知識を元に、問題を解きます。
問題文に「同じ温度でも」とあるので、飽和水蒸気量[g/m3]は一定であると考えることができます。
しかし、空気に含まれている水蒸気量[g/m3]が多いつまり露点(℃)が高いと、湿度(%)が高くなり、温度がわずかに下がっただけでも水蒸気が凝結して水滴となり、霧などになって現れます。
大問10 天気とその変化(中2・地学)
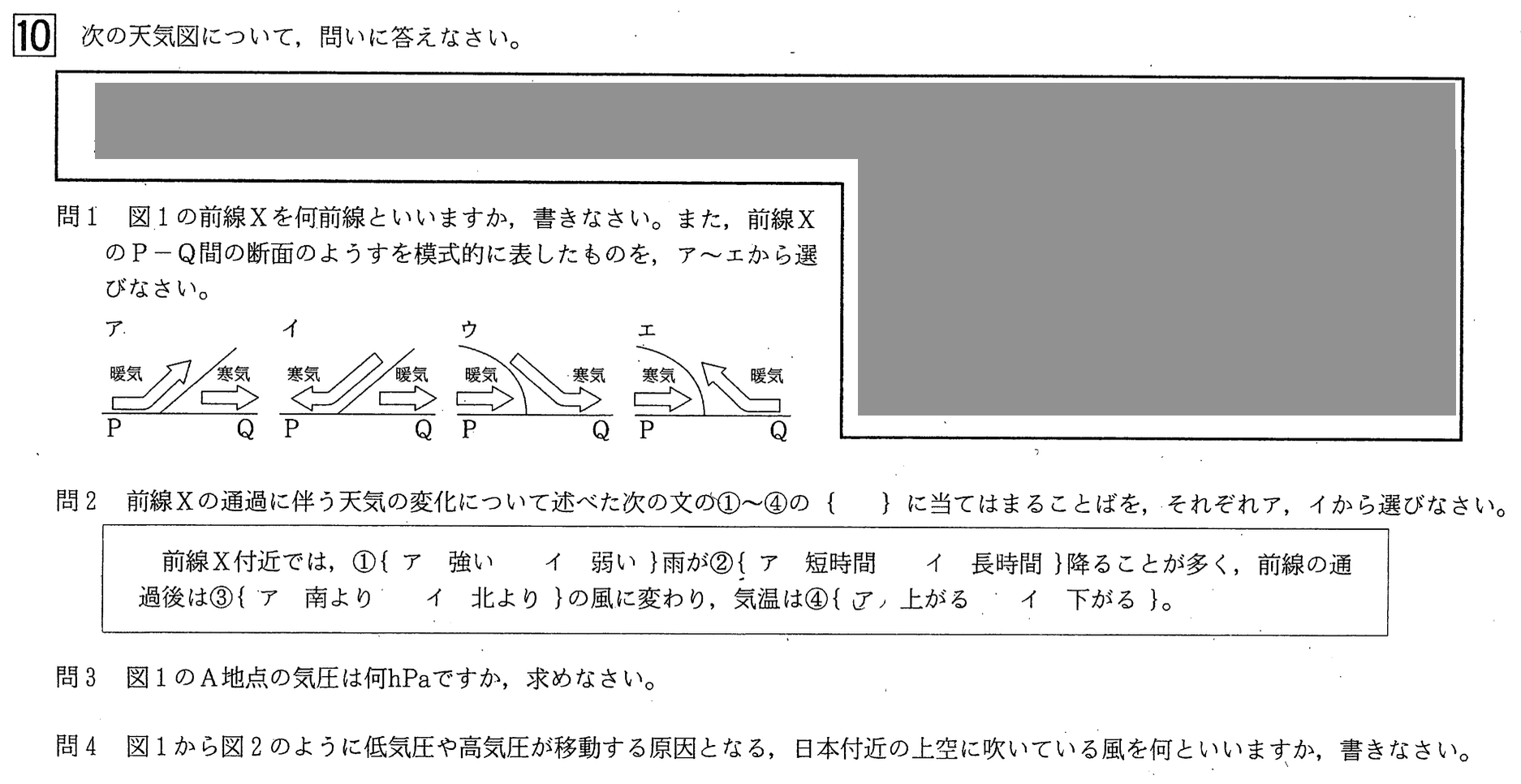
問1
解答:前線・・・寒冷(前線)、断面・・・エ
解説:
空気の成分比率は、体積の割合で多い順から
窒素(約78%)、酸素(約21%)、アルゴン(約0.9%)、二酸化炭素(約0.04%)です。
このほか、ネオン、ヘリウムなども微量ですが含まれています。
これらの気体分子(粒子)は、空気中を盛んに動いており、地面などに衝突して圧力(気圧)が生じます。
地面が太陽熱などで暖められると空気は上昇し、それと比較して冷たい場所に空気が流れ、空気が下降します。
空気が上昇すると、その場所では空気を構成する粒子の数が減るため、気圧が減少し、低気圧となります。
空気が下降すると、その場所では空気を構成する粒子が押されて数が増えるため、気圧が上昇し、高気圧となります。
空気は、冷たい方から温かい方に水平に流れます。
地球の地上10kmまでを対流圏といい、対流がさかんに起こっています。
対流のうち、水平方向の動きを風、垂直方向の動きを気流といいます。
暖かい場所では上昇気流が生じて低気圧となり、上昇した空気は冷たい方に流れ(風)、冷たい場所では下降気流が生じて高気圧となり、地表面では、暖かい場所(低気圧)から冷たい場所(高気圧)に向かって流れます(風)。
地球では、自転速度の差によって生じる右向きの力であるコリオリの力が発生するので、北半球の風向は、等圧線に対して垂直な方向よりも右にそれて吹きます。
そのため、低気圧では反時計回りに風が吹き込み、高気圧では時計回りに風が吹き出します。
北半球では、北緯30〜60度付近で吹く西寄りの風である偏西風が吹くので、低気圧は東から西に流れます。
低気圧が流れることで、暖気と寒気(緯度が上がると冷える)が触れ、寒冷前線と温暖前線が生じます。
この前線をともなう低気圧のことを、温帯低気圧といいます。
偏西風により低気圧は東から西に流れ、コリオリの力により風は低気圧に反時計回りに吹き込むことで、
温帯低気圧の左側で寒冷前線が、温帯低気圧の右側で温暖前線が生じます。
前線が通過する順番は、温暖前線→寒冷前線の順です。
温暖前線を正面から見ると、密度が小さく軽い暖気が密度が高く重たい寒気の上にはいあがり、寒気を後退させながら進みます。
このため緩やかな上昇気流が生じ、前線(暖気と寒気の境目である前線面と地面との接点)から右に向かって乱層雲・高層雲・巻層雲・巻雲などの層状の雲が生じ、乱層雲により広い範囲(前線から200〜300km)に長い時間、弱い雨を降らせます。
通過後は、暖気におおわれるため気温が上がり、風向が南よりに変わります。
寒冷前線を正面から見ると、密度が高く重たい寒気が密度が低く軽い暖気の下にもぐり込み、暖気を垂直方向に押し上げながら進みます。
このため激しい上昇気流が生じ、前線から左に向かって積乱雲や積雲などが生じ、積乱雲により狭い範囲(前線から50〜60km)に短時間で強い雨が降らせます。
通過後は、寒気に覆われるため気温が下がり、風向が南よりから北よりに急変します。
問2
解答:①・・・ア、②・・・ア、③・・・イ、④・・・イ
解説:
問1解説参照。
問3
解答:1028(hPa)
解説:
気圧の単位はhPa(ヘクトパスカル)です。
空気の成分比率は、体積の割合で多い順から
窒素(約78%)、酸素(約21%)、アルゴン(約0.9%)、二酸化炭素(約0.04%)です。
このほか、ネオン、ヘリウムなども微量ですが含まれています。
これらの気体分子(粒子)は、空気中を盛んに動いており、地面などに衝突して圧力(気圧)が生じます。
気圧の等しい地点を結んだときにできる線を、等圧線といいます。
等圧線は全体としてなめらかな曲線となり、途中で枝分かれしたり、消えてなくなったりすることはありません。
等圧線は、1000hPaを基準にして、4hPaごとに細い線が引かれ、20hPaごとに太い線が引かれます。
高気圧は、等圧線が丸く閉じている部分で、中心にいくほど気圧が高くなります。
低気圧は、等圧線が丸く閉じている部分で、中心にいくほど気圧が低くなります。
また低気圧は、等圧線の間隔がせまく、距離に対しての気圧の変化である気圧傾度が大きいため、風が強く吹き込みます。
以上の知識を元に、問題を解きます。
図のA地点は、1020hPaから低気圧から高気圧に向けて2本目にあるので、
気圧[hPa]=1020hPa+4hPa×2=1028hPa
問4
解答:偏西風
解説:
問1解説参照。
大問11 化学変化とイオン(中3・化学)

問1
解答:塩化水素
解説:
化学変化のうち、1種類の物質から、2種類以上の物質ができる変化を分解といいます。
分解には、熱分解と電気分解などがあります。
熱分解で覚えるのは、
・炭酸水素ナトリウムの熱分解
炭酸水素ナトリウム→炭酸ナトリウム+水+二酸化炭素
・酸化銀の熱分解
酸化銀→銀+酸素(2Ag2O→4Ag+O2)
・炭酸アンモニウムの熱分解
炭酸アンモニウム→アンモニア+水+二酸化炭素
電気分解で覚えるのは、
・水の電気分解
水→水素+酸素(2H2O→2H2+O2)
・塩酸の電気分解
塩酸→水素+塩素(2HCl→H2+ Cl2)
・塩化銅の電気分解
塩化銅→銅+塩素(CuCl2→Cu+Cl2)
気体の塩化水素が水に溶けた水溶液を、塩酸(化学式:HCl)といいます。
塩化水素は、無色・刺激臭がある有毒な気体で、水によくとけます。
塩化水素をアンモニア水に入れると、白煙が生じます。
塩酸の電気分解では、全体の反応(化学反応式)は以下のようになります。
2HCl → H2 + Cl2
水素(H2)と塩素(Cl2)の係数が1:1なので、体積比も1:1となり、水素と塩素が同じ体積分発生します。
しかし、陽極で塩素が発生する塩素は水に溶けやすいため、捕集できる量は塩素の方が少なくなります。
発生した気体の確認法として、陽極付近の水溶液に赤インクを加えると、塩素の漂白作用で赤色が脱色します。
塩酸の電気分解のメカニズムですが、まず、マイナスとプラスはくっつく、ということを押さえてください。
塩酸の電離式は、以下のとおりです。
HCl→H+ + Cl–
陽極(+極)には塩化物イオン(Cl–)が、陰極(−極)には水素イオン(H+)が移動します。
陽極(+極)では塩化物イオン(Cl–)が電子を2個放出し塩素(Cl2)が、陰極(−極)では移動してきた電子を水素イオン(H+)が受け取り水素(H2)が発生します。
問2
解答:HCl(→)H+(+)Cl–
解説:
問1解説参照。
問3
解答:電解質
解説:
水に溶かすとイオンに分かれる(電離する)物質を電解質といいます。
水に溶かしてもイオンに分かれず、粒子(分子)として水溶液中に拡散するだけの物質を非電解質といいます。
水中にイオンがあるので、電解質を溶かした水溶液(電解質の水溶液)は、電気(電流)を通します。
電解質として、酸、アルカリ、食塩、塩化銅などがあります。
非電解質として、砂糖とエタノールがあります。非電解質は砂糖とエタノールであることは、必ず覚えましょう。
問4
解答:水素・・・イ、塩素・・・ウ
解説:
代表的な気体の性質は、以下の通りです。
■酸素
酸素の性質として、以下の4つを押さえましょう。
①無色・無臭、②空気よりやや重い(空気の重さの約1.1倍)、③水にとけにくい、★④助燃性をもつ
酸素が発生する反応として、以下の例を覚えましょう。
・二酸化マンガンにうすい過酸化水素を加える
・過酸化水素を加熱する
・酸素系漂白剤にお湯を加える
・酸化銀を加熱する
・水を電気分解する
■水素
水素の性質として、以下の4つを押さえましょう。
①無色・無臭、②最も軽い気体(空気の重さの約0.08倍)、③水にとけにくい、★④可燃性をもつ
水素が発生する反応として、以下の例を覚えましょう。
・鉄にうすい塩酸を加える
・亜鉛にうすい塩酸を加える
・マグネシウムにうすい塩酸を加える
・水を電気分解する(水素イオンH+より、陰極で発生)
・塩酸を電気分解する(水素イオンH+より、陰極で発生)
■二酸化炭素
二酸化炭素の性質として、以下の4つを押さえましょう。
①無色・無臭、★②空気より重い(空気の重さの約1.5倍)、③水に少しとける(H+を放出する酸より水溶液は酸性)、★④石灰水を白く濁らせる
二酸化炭素が発生する反応として、以下の例を覚えましょう。
・石灰水にうすい塩酸を加える
・炭酸水素ナトリウムを加熱する
・炭酸水素ナトリウムにうすい塩酸を加える
・炭酸アンモニウムを加熱する
・酸化銅に炭素を加えて加熱する
■窒素
空気の約8割を占める窒素は、以下の5つの性質を持ちます。
①無色・無臭、②空気より少しだけ軽い、③水に溶けにくい、④助燃性(O2)・可燃性(H2)なし
★⑤常温では他の物質と結びついて化学変化を起こすことはほとんどない(この性質を利用した食品の酸化を防ぐ方法に、窒素充填がある)
■アンモニア
アンモニアの性質として、以下の4つを押さえましょう。
★①無色・刺激臭、★②空気より軽い、★③水に非常によく溶ける(20℃の水1cm3に702cm3溶ける)(OH–を放出するアルカリより水溶液はアルカリ性)→アンモニアの噴水実験、★④塩化水素と反応し、白煙(塩化アンモニウムの白色の固体)を生じる
アンモニアが発生する反応として、以下の例を覚えましょう。
・塩化アンモニウムと水酸化カルシウムの混合物を加熱する
・塩化アンモニウムと水酸化ナトリウムの混合物を加熱する(発熱反応)
・塩化アンモニウムと水酸化バリウムの混合物を加熱する
・炭酸アンモニウムを加熱する
このほか、塩素の性質も覚えましょう。
①黄緑色・刺激臭、②水に溶けやすい、③水溶液は酸性、④殺菌・漂白作用がある
大問12 生命の連続性(中3・生物)

問1
解答:ウ
解説:
からだをつくる細胞が分裂する細胞分裂を、体細胞分裂といいます。
植物の根の成長は、2段階で進みます。
第一段階では、根端分裂組織(根の成長点)でさかんに体細胞分裂が起こり、細胞の数を増やします。
第二段階では、分裂した細胞がもとの大きさくらいまで成長します。
体細胞分裂の観察実験では、タマネギを用いて、以下の手順で行われます。
①体細胞分裂は根の先端付近でさかんに行われるので、タマネギの根の先端を5mmくらい切る
②(省略可能)酢酸で固定する。固定とは、細胞を生きていた状態に近いまま殺し、細胞内の構造・物質の分解を防ぐ方法です。
③塩酸で細胞どうしを離す。これを解離といい、細胞壁間の接着物質を溶かし、細胞どうしを離れやすくします。
④水洗する
⑤染色液で染色する。染色液に含まれる酢酸で固定できるので、手順②は省略可能。
⑥柄つき針を使って、カバーガラスをかける。気泡が入らないようにすること。
⑦ろ紙ではさんで軽く押しつぶす。細胞どうしの重なりをなくし観察しやすくするため。
なお、スライドガラスの上に観察物をのせ、カバーガラスをかけたものをプレパラートといいます。
プレパラートを作成するときの注意点は、カバーガラスをかけるとき、中に気泡が入らないように、カバーガラスを端からゆっくり下ろすことです。
プレパラートは、ステージ上下式顕微鏡(鏡筒上下式顕微鏡)や双眼実体顕微鏡のステージの上に固定して、観察物を観察します。
問2
解答:(a→)b(→)e(→)c(→)d
解説:
体細胞分裂では、まず核分裂が起き、続いて細胞質分裂が起こります。
①間期:核1個あたりのDNA量が2倍になり、染色体が複製される(a)
②核膜と核小体が消失し(b)、染色体が短く太く凝縮して縦列する(e)
③染色体が中央に並ぶ
④染色体が両端に半分ずつ分裂する(c)
⑤分裂した染色体が核膜におおわれ、植物細胞では細胞板が中央から細胞質を分裂する(d)
問3
解答:染色体
解説:
核は、中に遺伝子をのせた染色体を持ちます。
染色体は、遺伝子の本体として働く物質であるDNAと、ヒストンというタンパク質からなる糸状の構造物で、染色液によく染まることから、染色体と名が付けられています。
(染色体の”染色”の名の由来)
染色液として、以下の3種類を覚えましょう。
・酢酸カーミン溶液(赤色に染まる)
・酢酸オルセイン溶液(赤紫色に染まる)
・酢酸ダーリア溶液(青紫色に染まる)
問4(悪問?)
解答:16(本)<32本も可>
解説:
図のcは細胞質分裂が行われた状態なので、細胞全体の染色体数が32本なら、上下の染色体数は、元の体細胞の染色体数の16本であることが分かります。
図のaは、染色体の複製が行われる間期か、染色体の複製が行われる前であるのか、図からは判断ができません。
染色体の複製が行われる前であるなら、元の体細胞の染色体数の16本であると言えます。
染色体の複製が行われる間期であるなら、元の体細胞の染色体数の16本の2倍の32本であると言えます。