👉教師紹介・料金
※授業料1回1,500円+交通費(コミコミ最大3,000円)・入会金なし・お好きな日時に受講・3回のお試し期間あり(無料教材あり)
>>的中率60%以上!今年度の北海道公立高校入試「理科」はここが狙われる!家庭教師のそらの予想出題分野
■ボーダー(合格)ライン・最低点の推移
>>北海道公立高校入試の道コン最低点推移のランク別まとめ
■平均点推移と予想
>>北海道公立高校入試の平均点推移・各科目の正答率・人数分布・平均点予想まとめ
■一般入試の合否判定の手順
>>【最新版】北海道公立高校一般入試の合否判定の手順の詳細まとめ
■一般入試(全体・学区外受験)の最終倍率推移
>>北海道公立高校入試の一般入試(全体・学区外受験)の最終倍率推移
北海道公立高校入試過去問はこちら
★過去問
★模擬テストとリスニング対策
※模擬テストは1教科のみ表示。Amazonなどでは5教科すべて販売されています。
大問1 小問集合
問1
(1)
(答)交流
直流と交流の違いは問題文ごと暗記しましょう。
交流は+−が周期的に変わるので、極性を持つLEDでは光のすじが破線になります。
極性を持たない豆電球は、連続した光のすじができます。
交流の周波数は、東日本では50Hz、西日本では60Hzです。
50Hzとは、1秒間に通過する電気や音の波の数(隣り合う山と山が1つの波)が50あるということです。
周波数の計算も出来るようになってください。
(2)
(答)食物
食物連鎖の用語について、問題文ごと暗記しましょう。
しかし、この知識だけでは小問しか解けないので、さらに突っ込んで勉強してください。
(3)
(答)自転
自転の用語について、問題文ごと暗記しましょう。
しかし、この知識だけでは小問しか解けないので、さらに突っ込んで勉強してください。
(4)
(答)酸
PHとは、0〜14のメモリをつけて、酸性・アルカリ性の度合いを表したものです。
7より小さいと酸性で、7より小さいほど酸性の度合いが強くなります。
食酢はPHが2〜3、塩酸はPHが0〜1です。
(5)
(答)遺伝
遺伝の用語について、問題文ごと暗記しましょう。
また、エンドウの子の形質と親の交配パターンを理解して覚えましょう。
とくに重要なのは、丸形の親としわ形の親を交配させたとき、子に丸としわの両方が現れる場合、丸形の親の遺伝子型は必ずAaになるという点です。
(6)
(答)日食
日食の概要については、問題文のとおりです。
日食は、月が新月(月齢0)のときに起こります。
地球は西から東に自転しているため、1日でみたら月と太陽は東から西に動いて見えます(見かけの動き)。
日食が起こるとき、月が最初に天体上に現れるのは暗記しましょう。
天体上で真南の方向を見ると、月と太陽は東から西に動いて見えますが、月は西から東に1日12°公転しているため、見かけの動きの速さは太陽のほうが大きいです。
ゆえに太陽が月に追いついて、太陽の右(西)側が欠けて右(西)側から満ちていきます。
これが日食のメカニズムです。
月が満月(月齢15)のときに起こる月食のときは、地球の影を太陽と見立てて、日食と同じように考えると、月の左(東)側が欠けて左(西)側から満ちていくことが分かります。
(7)
(答)組織液
血液は、固形成分の血球(赤血球・白血球・血小板)と、液体成分の血しょうからできています。
赤血球・白血球・血小板・血しょうのそれぞれの特徴を必ず押さえてください。
血しょうが毛細血管の外にしみ出て、細胞間を満たしている液を組織液といいます。
細胞呼吸で使われるブドウ糖・アミノ酸・脂肪・酸素、排出される二酸化炭素・水・アンモニアは、血しょうによって運搬されます。
(8)
(答)陽イオン
陽イオンと陰イオンについて、概要だけで良いので押さえてください。
主な原子や原子団のイオン式(15個ほどある)も、必ず覚えましょう。
これらイオン式を覚えることで、化学反応式や電離式がスムーズに理解できるようになります。
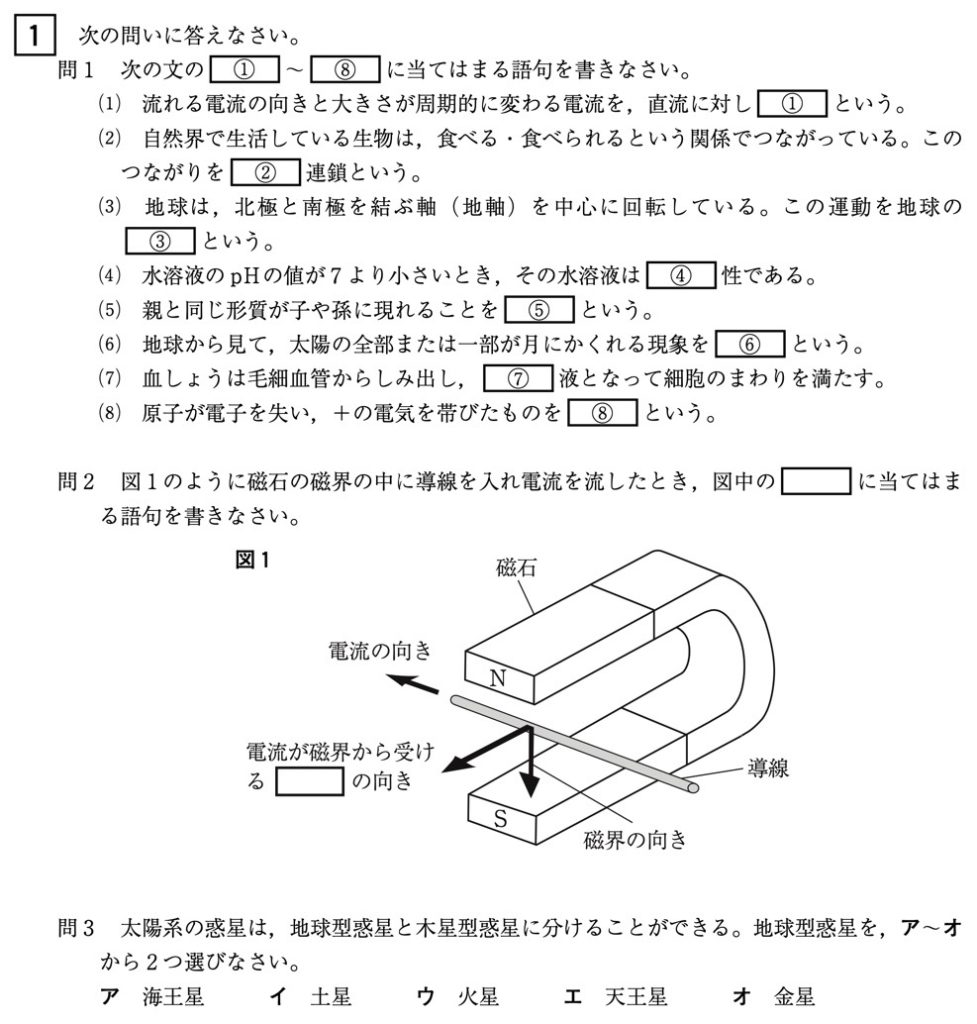
問2
(答)力
フレミング左手の法則の問題です。
磁界・電流の向きから、力の向きを即座に答えられるようになってください。
フレミング左手の法則の裏技として、『塾技 理科80』には「右手のパー」が紹介されています。
右手のパーを使うと、手を動かすまでもなく即座に力の向きが分かります。
問3
(答)ウ、オ
地球型惑星は、水星—金星—地球—火星、です。
木星型惑星は、木星—土星—天王星—海王星、です。
地球型惑星は質量や体積は小さいが、岩石でできているため密度が大きいです。
木星型惑星は質量や体積は大きいが、ガスでできているため密度が小さいです。
水星—金星—地球—火星—木星—土星—天王星—海王星、それぞれの惑星の特徴を押さえてください。
問4
(答)①イ、②塩素
電気分解の問題です。
塩化銅(CuCl2)の電離式から、陽極(+極)と陰極(−極)で発生する物質が分かります。
塩化銅(CuCl2)の電離式は、以下のとおりです。
CuCl2→ Cu2+ + 2Cl–
プラス(+)とマイナス(-)はくっつくが、プラス(+)とプラス(+)、マイナス(-)とマイナス(-)は反発し合います。
よって、塩化物イオン(Cl–)は陽極(+極)に行き塩素(Cl2)が、銅イオン(Cu2+)は陰極(−極)に行き銅(Cu)が発生します。
電気分解の概要は、こんな感じです。
電気分解のメカニズムについて、さらに突っ込んで勉強してください。
問5
(答)イ、エ
セキツイ動物は、魚類・両生類・ハチュウ類・鳥類・ホニュウ類の5つに大別されます。
魚類・両生類・ハチュウ類は、まわりの温度に応じて体温を変えることができる変温動物です。
鳥類・ホニュウ類は、まわりの温度が変化しても体温がほぼ一定に保たれる恒温動物です。
各選択肢を見ていくと、アのメダカは魚類、イのハトは鳥類、ウのミミズは無セキツイ動物、エのウサギはホニュウ類、オのイカは無セキツイ動物、カのトカゲはハチュウ類です。
以上から、答えは選択肢イとエになります。
ミミズは皮膚呼吸をすること、皮膚呼吸の内容について押さえてください。
イカについて、分類のし方(外とう膜の有無で分類)や身体のつくりなど、詳しく勉強してください。
問6
(答)2A
オームの法則より、電熱線に流れる電流=回路全体に流れる電流は、以下のように計算できます。
V=IR⇔I=V/R=6V/3Ω=2A
問7
(答)C、D
等圧線は4hPaごとに区切り、20hPaごとに太い線が引かれます。
また、高気圧は中心にいくほど気圧が高くなり、低気圧は中心にいくほど気圧が低くなります。
C地点とD地点は1020hPaの高気圧側にあるので、1020hPaより気圧が高いです。
A地点とB地点は1020hPaの低気圧側にあるので、1020hPaより気圧が低いです。
大問2 植物の生活と種類(生物分野・中1)


問1(1)
(答)イ
あたためたエタノールにつける目的は、葉の緑色を脱色し、ヨウ素液の色の変化を見やすくするためです。
問1(2)
(答)直接加熱してはいけない
教科書に書かれている内容です。
こういう問題にも対処できるよう、教科書も必ず2〜3読してください。
問2
(答)①イ、②ア
問題文に書かれている内容どおりです。
なお、暗室に1日置く目的は、葉のデンプンを無くすためです。
暗室に1日置いた後に光を当てることで、葉は光合成によりデンプンを作ることが確かめられます。
デンプンはヨウ素液と反応して青紫色になります。
問3(1)
(答)
試験管S:ア
試験管U:ウ
BTB溶液は、アルカリ性では青色、中性では緑色、酸性では黄色になります。
問題文のBTB溶液は、息を吹き込んで緑色にしていることから、元はアルカリ性です。
息を吹き込むと、BTB溶液に二酸化炭素が溶け、液は酸性に傾きます。
試験管Uですが、ホウセンカをアルミニウムはくで覆っていることから、ホウセンカは呼吸のみします。
呼吸により二酸化炭素が放出され、緑色のBTB溶液に二酸化炭素が溶け、液はさらに酸性に傾き、黄色になります。
以上から、試験管Uの答えは選択肢ウになります。
試験管Sですが、ホウセンカに光を当てていることから、ホウセンカは光合成と呼吸をします。
光合成は二酸化炭素量が消費され、呼吸では二酸化炭素量が放出されます。
図2で試験管SのBTB溶液の上部が青色になっているのは、光合成で消費される二酸化炭素量が、呼吸で放出される二酸化炭素を上回り、液に溶けていた二酸化炭素が消費されてアルカリ性に戻ったからです。
以上から、試験管Sの答えは選択肢アとなります。
問3(2)
(答)
[Ⅰ群]:ア
[Ⅱ群]:ク
光の強さと光合成量・呼吸量についての問題です。
光の強さと放出・吸収される酸素量のグラフの知識を覚えましょう。
[Ⅰ群]試験管Uより、呼吸により葉が放出した二酸化炭素量Yは10と表すことができます。
試験管Tについて、葉の見かけの光合成量は1なので真の光合成量は11になります。
葉は呼吸により放出した二酸化炭素量10と、BTB溶液中の二酸化炭素量1、合計で二酸化炭素量11を吸収して光合成を行っています。
以上から、光合成により葉が使った二酸化炭素量Xは11と表すことができます。
X(11)>Y(10)なので、答えは選択肢アとなります。
[Ⅱ群]試験管Sについて、葉の見かけの光合成量は3なので真の光合成量は13になります。
葉は呼吸により放出した二酸化炭素量10と、BTB溶液中の二酸化炭素量3、合計で二酸化炭素量13を吸収して光合成を行っています。
以上から、光合成により葉が使った二酸化炭素量Zは13と表すことができます。
Z(13)>X(11)なので、答えは選択肢クとなります。
問4
(答)より多くの二酸化炭素を使い、デンプンをたくさんつくる
実験1から分かることは、葉は光を当てると光合成を行い、デンプンを生成するということです。
実験2から分かることは、葉は光を当てると二酸化炭素を吸収し、光の強さが強くなると吸収される二酸化炭素量が多くなるということです。
以上から、答えが導けます。
植物は光合成によりデンプンを生成し、デンプンは水に溶けやすい物質に変えられ、夜間に師管を通ってからだの各部に運ばれ、呼吸や成長の材料として使われます。
大問3 大地の変化(地学分野・中1)

問1
(答)かぎ層
柱状図の問題では、かぎ層として凝灰岩の層が使われます。
凝灰岩の層は、火山灰が滞積してできます。
問2
(答)ウ
石灰岩は、貝・サンゴ・フズリナの遺がいなどが堆積してできます。
サンゴは示相化石で、サンゴがあると当時の自然環境が「あたたかくて浅い海」であったことが分かります。
問3
(答)①ア、②イ
造岩鉱物である石英やチョウ石は白っぽい色をしています。
白っぽい鉱物の割合が多いと二酸化ケイ素の割合も多くなるので、火山灰の元であるマグマの粘り気が大きく、噴火は爆発的噴火、火山の形はドーム状(溶岩ドーム)となります。
黒っぽい鉱物割合が多いと二酸化ケイ素の割合も少なくなるので、マグマの粘り気が小さく、噴火はおだやか、火山の形は傾斜がゆるやかな形(盾状火山)となります。
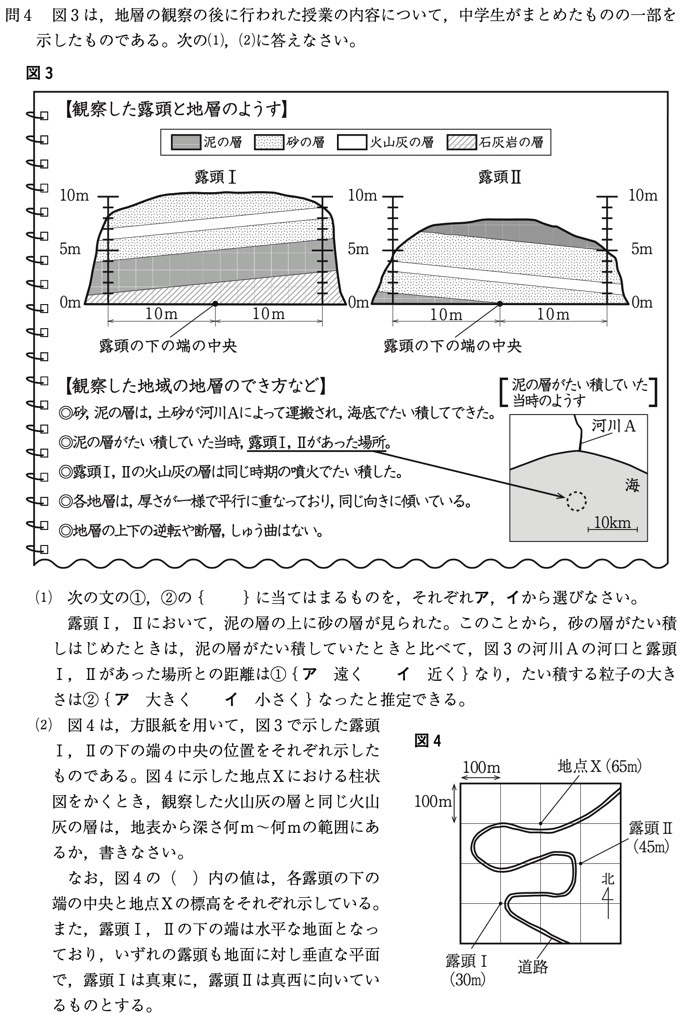
問4(1)
(答)①イ、②ア
上の層にいくほど粒が大きくなっていることから、海面の下降または海底の隆起が起こっていることが分かります。
このとき、地層と河口との距離は近くなります。
堆積岩であるれき岩、砂岩、泥岩は粒の大きさで分類されます。
粒の直径が2mm以上がれき岩、2〜1/16mmが砂岩、1/16mm以下が泥岩です。
問4(2)
(答)7m〜8m
まずかぎ層である凝灰岩の層(火山灰の層)の上面の標高を求めます。
露頭Ⅰ:30m+8m=38m
露頭Ⅱ:45m+3m=48m
問題文で「各地層は厚さが一様で平行に重なっており、同じ向きに傾いている」とあるので、露頭Ⅰと露頭Ⅱは南北に10m(48m-38m)傾いていると考えます。
すると地点Xの凝灰岩の層の上面の標高は58mとなり、地点Xの標高は65mで凝灰岩の層の厚さは1mから、凝灰岩の層は地表から7〜8mの深さにあると考えられます。
大問4 物質の成り立ち(化学分野・中2)

問1
(答)①熱分解、②H
実験1は、炭酸水素ナトリウムの熱分解のはなしをしています。
炭酸水素ナトリウムの熱分解の化学反応式は、以下のとおりです。
炭酸水素ナトリウム→炭酸ナトリウム+水+二酸化炭素
(2NaHCO3→Na2CO3+H2O+CO2)
炭酸水素ナトリウム(NaHCO3)に含まれ、炭酸ナトリウム(Na2CO3)に含まれない原子は水素原子(H)です。
問2(1)
(答)水
塩化コバルト紙が青色→赤色に変化したことから、熱分解により水が発生したことが分かります。
炭酸水素ナトリウムの熱分解では、炭酸ナトリウムと水と二酸化炭素が発生しますが、それぞれの物質の確認法は以下のとおりです。
・炭酸水素ナトリウム:フェノールフタレイン溶液を加えるとうすい赤色(水に少し溶けるため)
・炭酸ナトリウム:フェノールフタレイン溶液を加えると濃い赤色(水によく溶けるため)
・水:塩化コバルト紙が青色から赤色に変化
・二酸化炭素:石灰水が白く濁る
問2(2)
(答)①二酸化炭素、②カルシウム、③ア、④イ
問2(1)解説より、石灰水が白く濁るとき、二酸化炭素が発生したことが分かります。
石灰水(水酸化カルシウム、アルカリ性)に二酸化炭素(酸性)を加えると中和が起こり、塩として水に溶けにい炭酸カルシウムが発生します。
石灰水が白く濁るのは、炭酸カルシウムのせいです。
石灰水に含まれているカルシウムと水酸化バリウムに含まれているバリウムは、周期表のタテ(族)が同じで、性質が似ています。
水酸化バリウム水溶液に二酸化炭素を加えると中和が起こり、塩として塩として水に溶けにい炭酸バリウムが発生し、水溶液が白く濁ります。
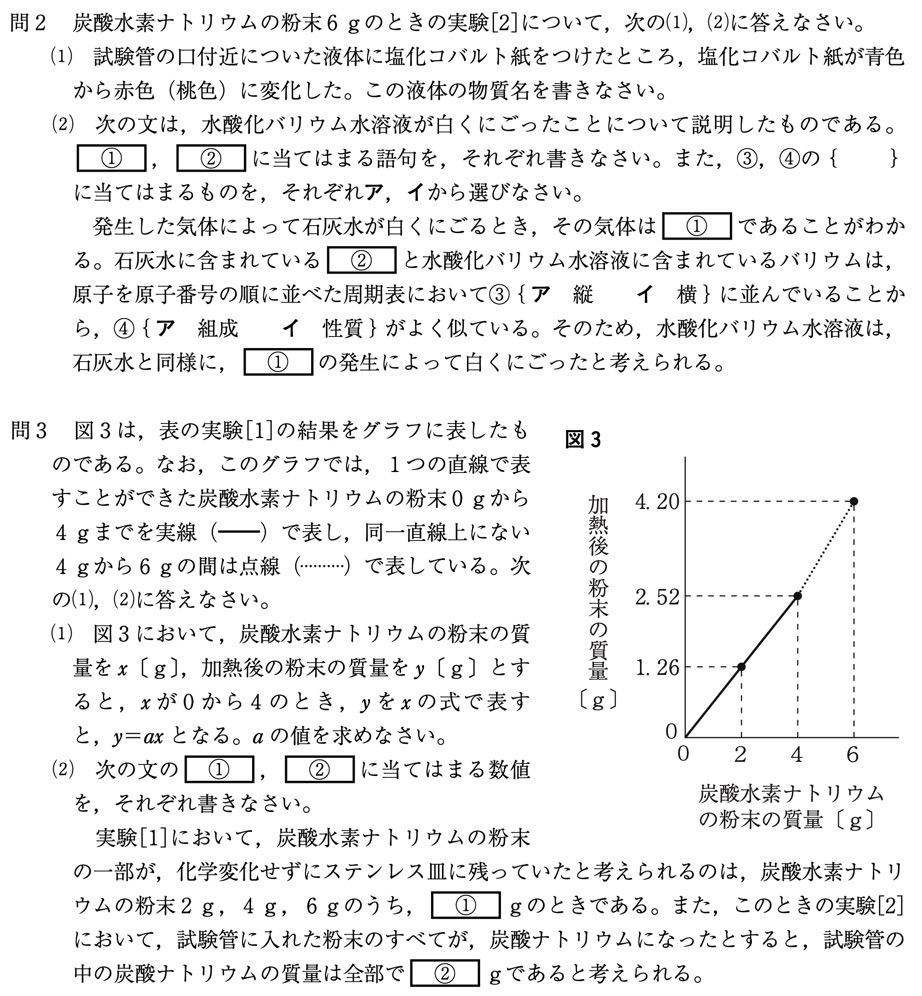
問3(1)
(答)0.63
0≦x≦4のとき、原点を通る直線になります。
xの増加量が2のとき、yの増加量は1.26となるので、傾きは1.26/2=0.63となります。
問3(2)
(答)①6、②0.9
①
表より、炭酸水素ナトリウムの粉末が6gのとき、ステンレス皿で加熱後に1g採取して試験管で加熱したら、水と二酸化炭素が発生していることが分かります。
炭酸水素ナトリウムの熱分解では、炭酸ナトリウムと水と二酸化炭素が発生します。
ゆえに、炭酸水素ナトリウムの粉末が6gのとき、炭酸水素ナトリウムが残っていたと考えられます。
②
過去最高難度の難問です。
まず、問題文の表を以下のようにまとめます。
表
| 炭酸水素ナトリウムの粉末(g) | 2 | 4 | 6 |
| 加熱後の粉末の質量(g) | 1.26 | 2.52 | 4.20 |
| 発生した水と二酸化炭素の質量(g) | 0.74 | 1.48 | 1.8 |
炭酸水素ナトリウムの粉末が2gと4gのとき、炭酸水素ナトリウムが全て熱分解しています。
炭酸水素ナトリウムの粉末が2gから4gと2倍に増えたとき、発生した二酸化炭素と水の質量は0.74gから1.48gと2倍に増えています。
炭酸水素ナトリウムの粉末が6gのとき、炭酸水素ナトリウムが全て熱分解したら、二酸化炭素と水は0.74×3=2.22g発生することになります。
炭酸水素ナトリウムの粉末が6gのとき、発生した二酸化炭素と水の質量が1.8gなので、あと0.42g発生することができます。
炭酸水素ナトリウムの粉末が2gが過不足なくすべて反応すると二酸化炭素と水は0.74g発生するので、二酸化炭素と水の質量が0.42g発生するときの炭酸水素ナトリウムの質量は、以下の比例式で表されます。
2:0.74=x:0.42
x=(2×42)/74
加熱後の粉末4.20gに含まれている炭酸ナトリウムの質量は、
4.2-(2×42)/74=(4.2×74-4.2×20)/74=(4.2×54)/74
炭酸水素ナトリウム2gが過不足なく反応すると1.26gの炭酸ナトリウムが発生するので、加熱後の粉末4.20gに含まれている炭酸水素ナトリウムが全て反応するときに発生する炭酸ナトリウムの質量は、
2:1.26=(2×42)/74:x
x=(1.26×42)/74
ゆえに、炭酸水素ナトリウム6gが過不足なく反応したときに発生する炭酸ナトリウムの質量は、
(4.2×54)/74+(1.26×42)/74=(4.2×54+4.2×12.6)/74=(4.2×66.6)/74
炭酸水素ナトリウム6gのとき加熱後の粉末の質量は4.2gで、その中から1g採取することから、上の式を4.2で割って炭酸ナトリウムの質量が求まります。
66.6/74=0.9
(別解)
表より、炭酸水素ナトリウムの粉末が6gのとき、発生した二酸化炭素と水の質量が1.8gなので、あと0.42g発生することができます。
加熱後の粉末4.2gから1gを採取すると、この粉末からあと0.1g(0.42g÷4.2g)の二酸化炭素と水が発生することになります。
ゆえに、採取した1gを試験管で加熱後に残る粉末の質量は0.9gで、二酸化炭素と水が全て発生したことから、この粉末は全て炭酸ナトリウムであるといえます。
大問5 運動とエネルギー(物理分野・中3)


問1(1)
(答)エ
50打点で1秒なので、5打点で0.1秒です。
5打点目のとき、0打点目からの距離が3.5cmなので、台車は0.1秒間に3.5cm進んだことになります。
ゆえに、平均の速さ(cm/秒)は、
平均の速さ(cm/秒)=3.5cm/0.1秒=35cm/秒
問1(2)
(答)エ
台車が斜面を移動する運動なので、等加速度運動です。
等加速度運動では、時間と速さのグラフが与えられていれば、三角形の面積を求めることで距離を求めることができます。
しかし表から分かるのは平均の速さのみで、その点での速さは不明なのでこの方法は使えません。
表を以下のように作り替えます。
表
| 打点(打点目) | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
| 時間(秒) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 |
| 0打点目からの距離(cm) | 3.5 | 9.7 | 18.6 | 30.2 | 44.5 | 61.5 | x |
| 距離の増加量(cm) | – | 5.2 | 8.9(+2.7) | 11.6(+2.7) | 14.3(+2.7) | 17(+2.7) | 19.7(+2.7) |
以上から、0打点目から35打点目までの距離は、
x=61.5+19.7=81.2cm
と求められます。
問1(3)
(答)イ
台車は同一斜面上を移動するので、結果は実験1の表と同じくなります。
表では、0打点目からの距離が30.2cmのとき打点は20打点なので、答えは20打点です。
問2(1)
(答)①ア、②イ
①
図より、斜面X(台車Ⅰ)のほうが斜面Y(台車Ⅱ)より傾きが大きいので、台車Ⅰのほうが速さの増え方が大きくなります。
②
斜面Y(台車Ⅱ)は斜面X(台車Ⅰ)より長く、傾きが小さく速さの増え方が斜面X(台車Ⅰ)より小さいので、D点—R点のラインに到達するのにかかる時間は、台車Ⅱの方が大きくなります。
問2(2)
(答)ア
A点とD点は同一斜面上にあるので、台車に働く斜面方向の分力は同じです。
台車に働く斜面方向の分力は、斜面の傾きが大きいほど大きくなります。
問2(3)
D点—R点のラインを基準面とすると、図4よりA点P点での位置エネルギーの大きさは3となります。
A点P点では台車の速さがゼロなので、力学的エネルギーの大きさは3です。
Q点はP点—R点間の高さの半分なので、Q点での位置エネルギーの大きさは1.5となります。
Q点での運動エネルギーの大きさは、力学的エネルギーから位置エネルギーの大きさを引いて、1.5です。
B点はA点—D点間の高さの2/3の点なので、位置エネルギーの大きさは2です。
B点での運動エネルギーの大きさは、力学的エネルギーから位置エネルギーの大きさを引いて、1です。
ゆえに、Q点での運動エネルギー(1.5)は、B点での運動エネルギー(1)の1.5倍です。
図解すると、以下のようになります。