★高専入試オススメ過去問題集★
大問1 小問集合
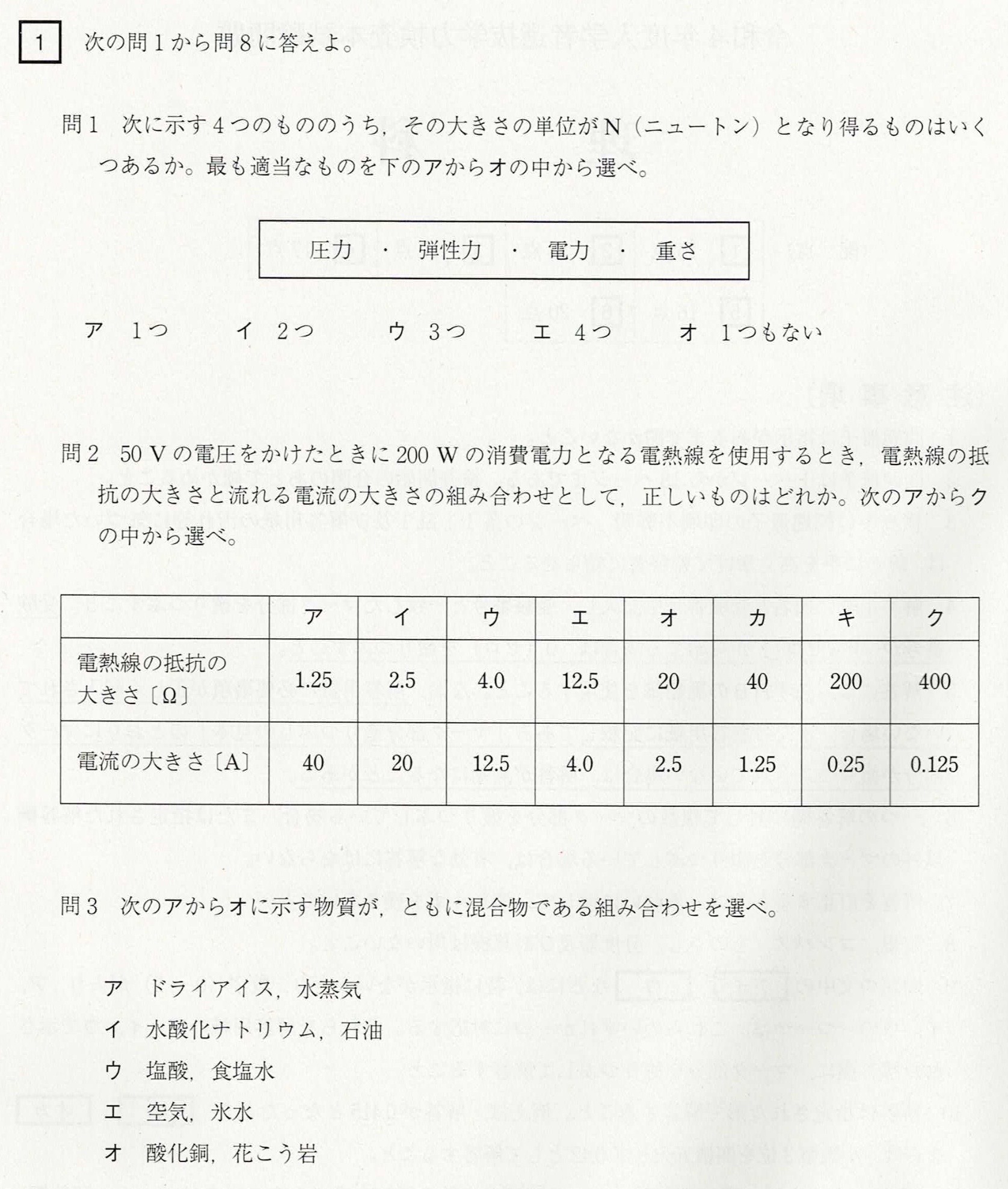


問1
解答:イ
解説:
圧力の単位は[N/m2]、弾性力の単位は[N]、電力の単位は[W]=[J/s]、重さの単位は[N]です。
問2
解答:エ
解説:
消費電力P[W]=I[A]×V[V]
これより、電圧V[V]=200W÷50V=4Aとなります。
オームの法則より、抵抗R=V/I=50V/4A=12.5Ωです。
問3
解答:ウ
解説:
ア:ドライアイスは二酸化炭素、水蒸気は水のみで構成される化合物(純物質)です。
イ:水酸化ナトリウムは化合物(純物質)ですが、石油は混合物です。
ウ:正しい。塩酸は、気体の塩化水素が水にとけたものなので、塩化水素と水の混合物です。食塩水は、塩化ナトリウムが水にとけたものなので、塩化ナトリウムと水の混合物です。
エ:空気は混合物ですが、氷水は水のみで構成されるので化合物(純物質)です。
オ:酸化銅は化合物(純物質)、花こう岩は混合物です。
問4
解答:エ
解説:
水の電気分解の化学反応式は、
2H2O → 2H2 + O2
水素分子は水素原子が2個結合、酸素分子は酸素原子が2個結合したものです。
問5
解答:イ
解説:
ステージ上下式顕微鏡の使い方は、明るくしてから(①)対物レンズを近づけて(③)、対物レンズを遠ざけてピントを合わせます(②)。
問6
解答:ウ
解説:
単純な知識問題なので、解説略。
問7
解答:イ
解説:
温暖前線通過後は暖気に覆われるため、気温は上がります。
低気圧は風が反時計回りに吹き込むため、温暖前線通過後は風向が南寄りになります。
問8
解答:ア
解説:
ア:誤り。一日の中で気温が最も高くなるのが正午より遅れる理由は、太陽からの放射が地面を温めるのに時間がかかるためです。
大問2 炭酸水素ナトリウムの性質
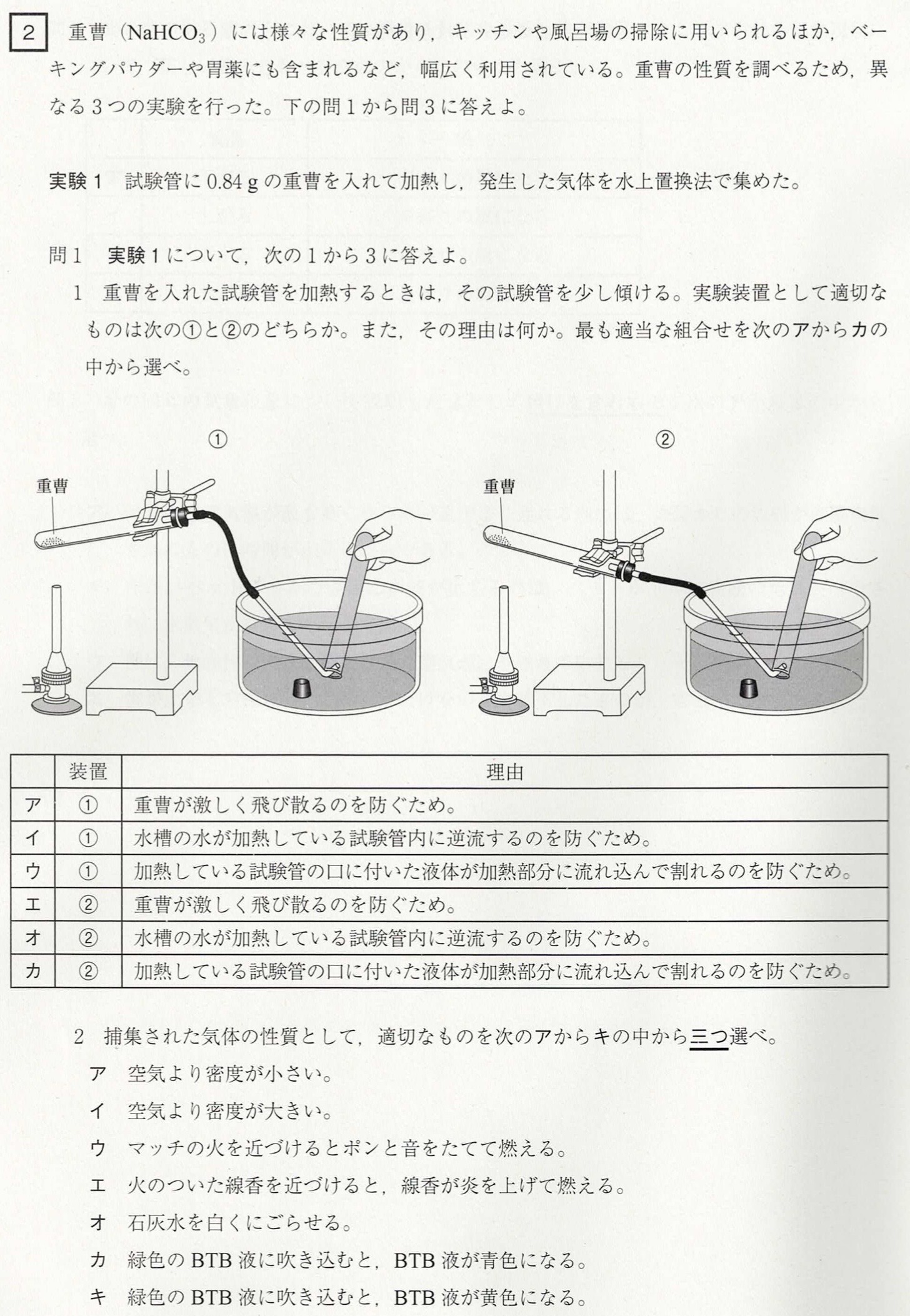
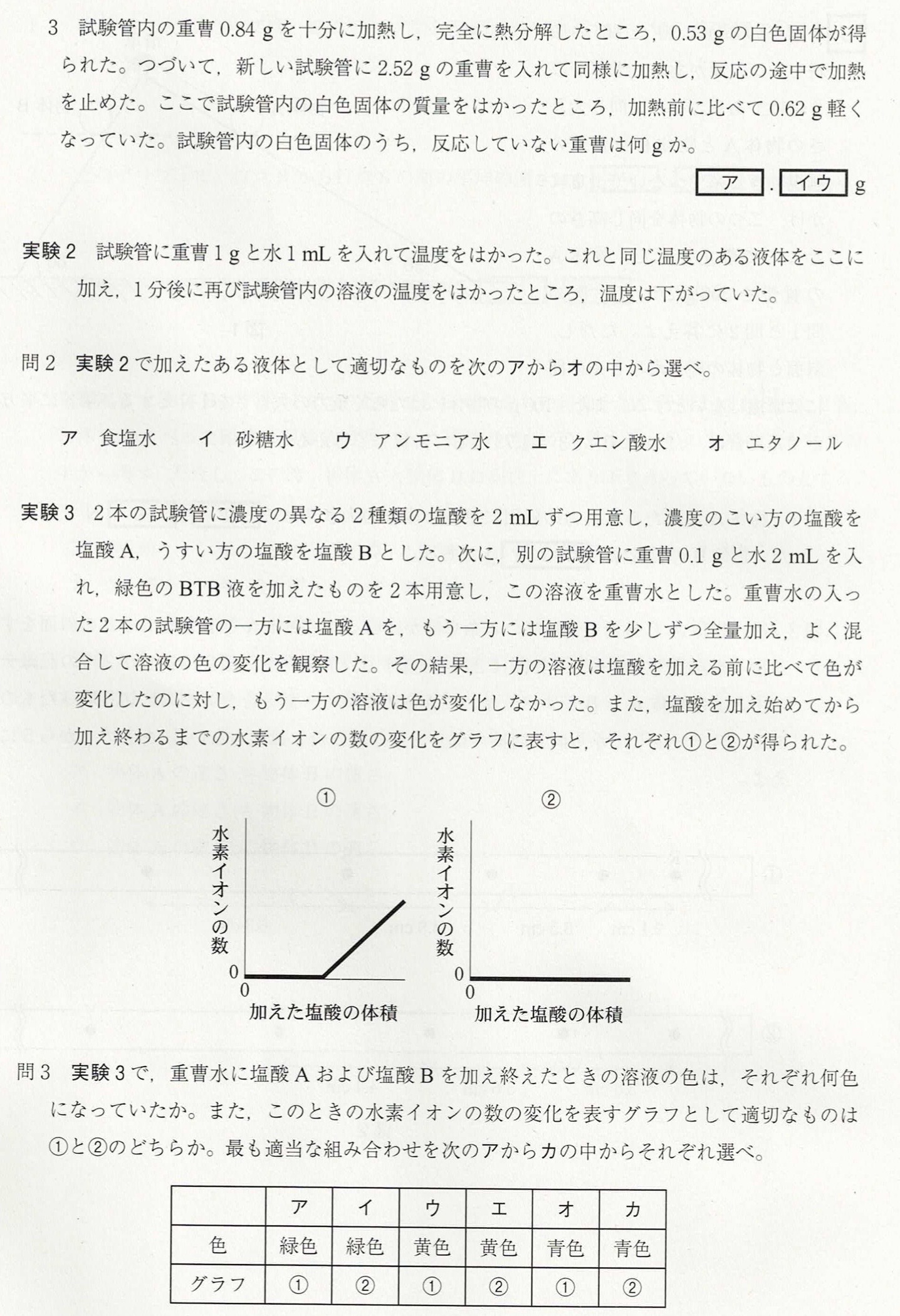
問1-1
解答:カ
解説:
重曹は炭酸水素ナトリウムです。
炭酸水素ナトリウムの熱分解により、液体として水が生じます。生じた水が過熱部に触れると試験管が割れて危険なので、②のように試験管を傾けます。
問1-2
解答:イ、オ、キ
解説:
炭酸水素ナトリウムの熱分解により、気体として二酸化炭素が生じます。
二酸化炭素は、空気の1.5倍重い(密度が大きい)(イ)です。
二酸化炭素は、石灰水(水酸化カルシウム)と中和し炭酸カルシウムの塩が生じます。炭酸カルシウムは水に溶けにくい白色の物質なので、石灰水が白く濁ります(オ)。
二酸化炭素が水に溶けると水素イオンが生じて酸性の水溶液になるので、BTB液が黄色になります(キ)。
問1-3
解答:ア・・・0、イ・・・8、ウ・・・4
解説:
炭酸水素ナトリウムの熱分解により、固体として炭酸ナトリウムが生じます。
問題文の条件より、炭酸水素ナトリウム0.84gが完全に反応すると、炭酸ナトリウムが0.53g、水と二酸化炭素が0.31g(0.84g – 0.53g=0.31g)生じます。
2.52gの炭酸水素ナトリウムを加熱したら、0.62g=0.31g×2の水と二酸化炭素が生じているので、炭酸水素ナトリウムは0.84g×2=1.68g反応しています。
これより未反応の炭酸水素ナトリウムは、2.52g – 1.68g=0.84gです。
問2
解答:エ
解説:
炭酸水素ナトリウム(弱アルカリ性)とクエン酸(弱酸性)が反応すると中和が起こり、塩として生じた炭酸ガスが周囲の熱を奪います(吸熱反応)。
問3
解答:塩酸A・・・ウ、塩酸B・・・カ
解説:
実験により、弱アルカリ性の炭酸水素ナトリウムと酸性の水溶液である塩酸が反応して、中和が起こります。
塩酸Aを加えた場合(①のグラフ)では水素イオンが生じています。つまり、炭酸水素ナトリウムの水酸化物イオンの数より、塩酸の水素イオンの数の方が多いため、中和が起こると、水素イオンが残ります。水溶液に水素イオンがあるので、酸性の水溶液なので、BTB液は黄色になります。
塩酸Bを加えた場合(①のグラフ)では水素イオンは生じていません。つまり、炭酸水素ナトリウムの水酸化物イオンの数が、塩酸の水素イオンの数以上あるため、中和が起こると、水素イオンは残らないと考えられます。この段階では、BTB液の色が緑色か青色なのか分かりません。
問題文より、炭酸水素ナトリウム水溶液(弱アルカリ性)に緑色のBTB液を加えているので、BTB液は青色になります。問題文に「もう一方の溶液(塩酸Bを加えた)は色が変化しなかった(青色のまま)」とあるので、塩酸Bを加えた水溶液には水酸化物イオンが残っていることが分かります。よって、塩酸Bの正解はカです。
スポンサーリンク
大問3 物体の運動<難>
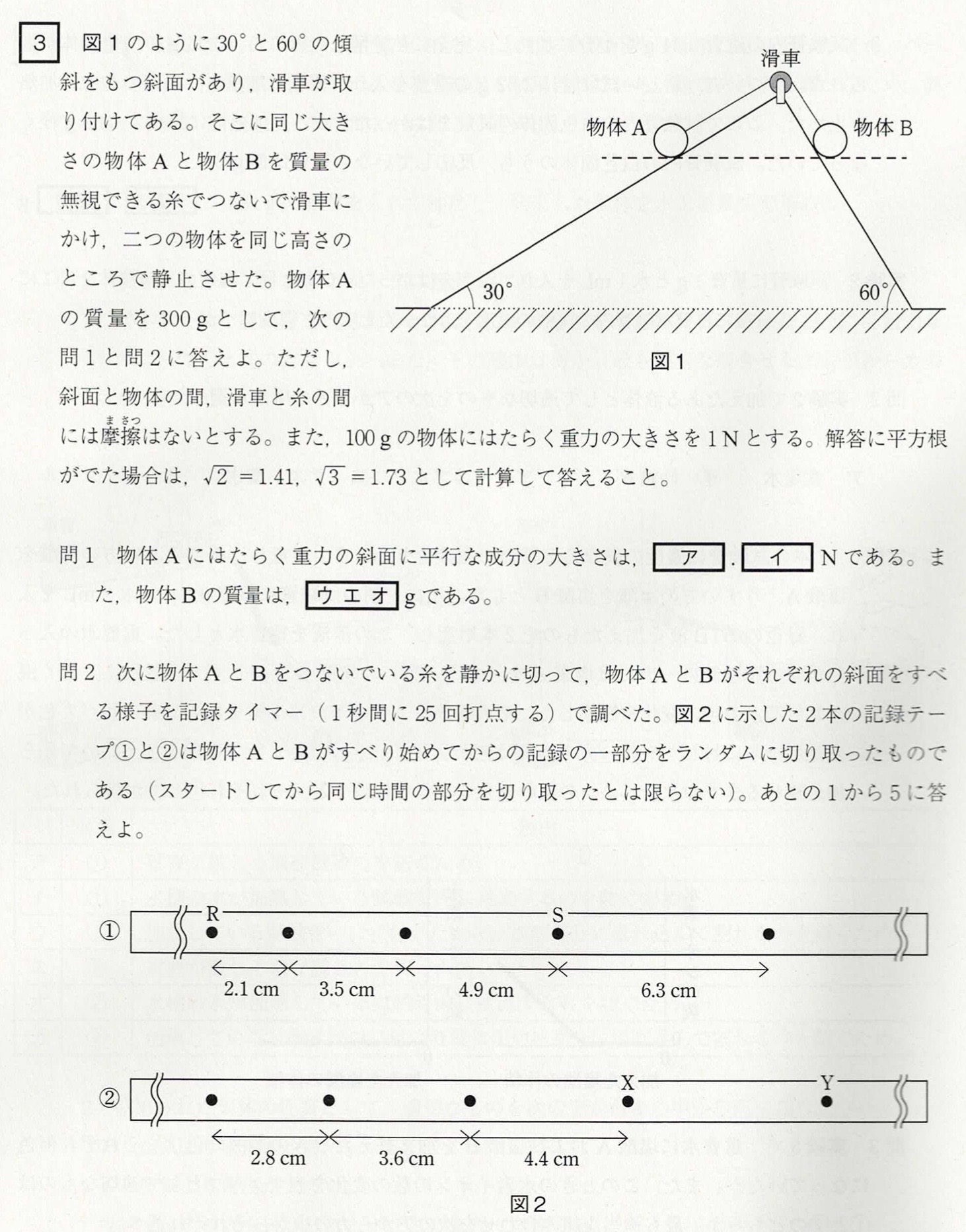

問1
解答:ア・・・1、イ・・・5、ウ・・・1、エ・・・7、オ・・・3
解説:
物体Aにはたらく重力の斜面方向の分力=重力×(高さ/斜辺)=3N×1/2=1.5N
物体Bにはたらく重力の斜面方向の分力=物体Aにはたらく重力の斜面方向の分力より、
物体Bにはたらく重力×(√3/2)=1.5N
物体Bにはたらく重力=1.5N×2/√3=3/√3=√3N
物体Bの質量=√3N×100g/N=1.73×100=173g
問2-1
解答:2
解説:
物体A側の方が斜面の傾きが緩やかなので、物体Aにはたらく重力の斜面方向の分力が小さいので、速さの増え方が物体Aの方が小さいです。
記録テープの打点間隔の広がり方が小さいと、速さの増え方が小さいので、物体Aの記録テープは②です。
問2-2
解答:ア・・・8、イ・・・7、ウ・・・5
解説:
R-S間の距離は、2.1+3.5+4.9=7.0+3.5=10.5cmです。
R-S間の時間は、(1s/25打点)×3打点=3/25sです。よって、
平均の速さ=10.5cm÷3/25s=10.5×25/3=3.5×25=(3+0.5)×25=75+12.5=87.5cm/s
問2-3
解答:ア・・・5、イ・・・2
解説:
打点間隔が0.8cmずつ増えているので、4.4cm+0.8cm=5.2cm
問2-4
解答:オ
解説:
糸を切ってから同じ時間だけ斜面を滑ったことから、運動方程式を用いて加速度を計算することで速度と移動距離が分かります。
物体Aの加速度=1.5N/300g=1.5/300m/s2
物体Bの加速度=1.5N/173g=1.5/173m/s2
物体Aの移動距離:物体Bの移動距離=1.5/300m/s2:1.5/173m/s2=173:300≒1:1.73
物体Bのすべった距離は物体Aの1.73倍なので、選択肢の中で最も近いのはオです。
問2-5
解答:イ
解説:
図1より、物体Aと物体Bの高さは等しいので、位置エネルギーの比は重力の大きさの比になります。
物体Aの位置エネルギー:物体Bの位置エネルギー=3N:1.73N
物体Aと物体Bの高さは等しいので、斜面最下端での運動エネルギーの比は、斜面上端での位置エネルギーの比と等しくなるので、
物体Aの運動エネルギー:物体Bの運動エネルギー=3N:1.73N
1.73×物体Aの運動エネルギー=3×物体Bの運動エネルギー
1.73×{1/2×300g×(物体Aの速さ)2}=3×{1/2×173g×(物体Bの速さ)2}=300×1/2×1.73g×(物体Bの速さ)2
(物体Aの速さ)2=(物体Bの速さ)2
物体Aの速さ、物体Bの速さはともに正の値だから、
物体Aの速さ=物体Bの速さ
スポンサーリンク
大問4 地学総合問題(岩石と惑星)

問1-1
解答:ア
解説:
花こう岩は無色鉱物の割合が多い、白色の深成岩です。
深成岩は等粒状組織より、鉱物の大きさが大きいため、目が粗く見えます。
問1-2
解答:ウ、エ
解説:
三葉虫とフズリナは古生代、アンモナイトと恐竜は中生代、ビカリアとナウマンゾウは新生代の生物です。
問1-3
解答:エ
解説:
選択肢の中で防湿性と耐火性が要求されそうなものは、倉や倉庫です。
問2-1
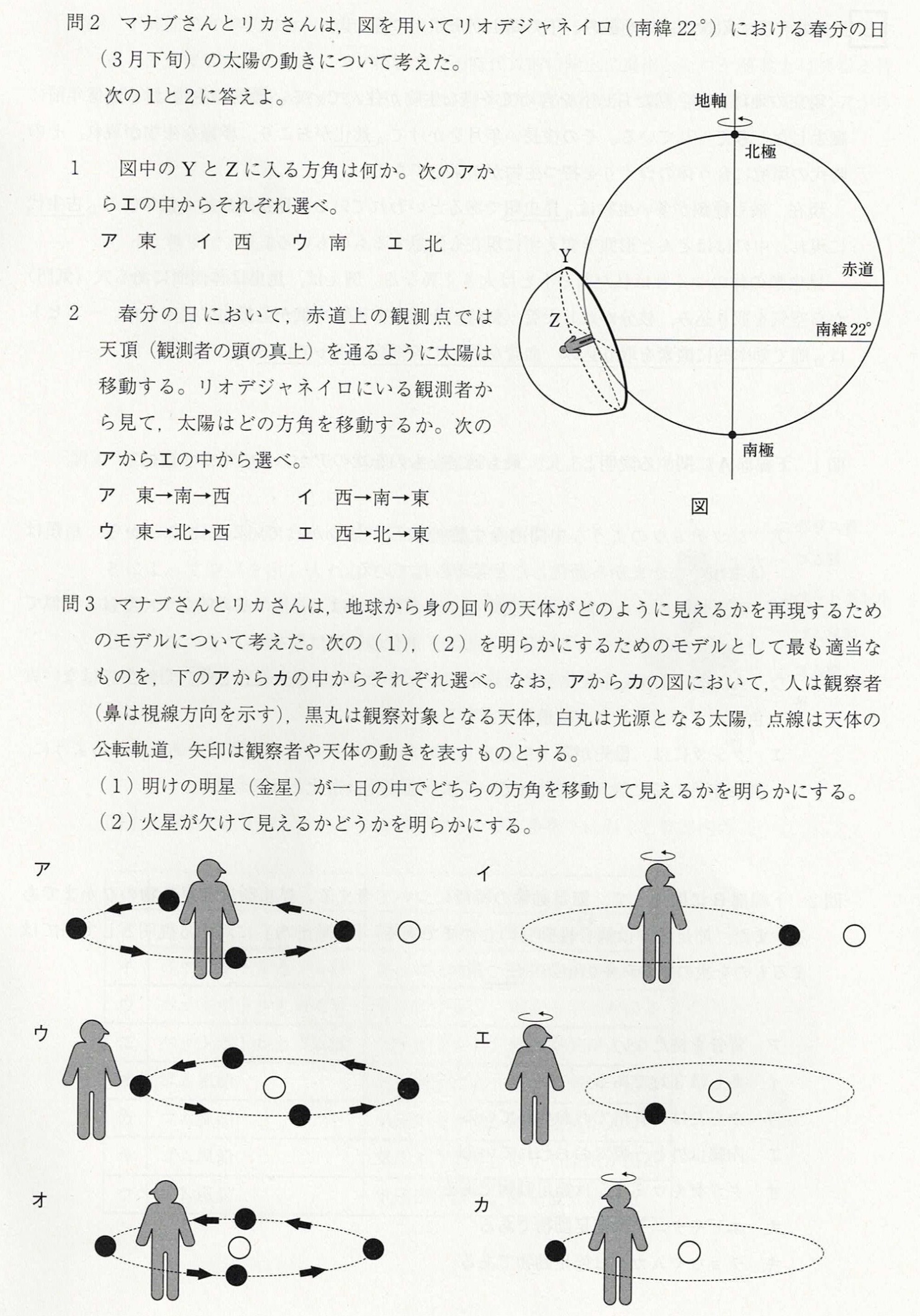
解答:Y・・・エ、Z・・・イ
解説:
地軸の北極側が北であるので、Yは北、Zは西です。
問2-2
解答:ウ
解説:
太陽は東から昇り西へ沈みますが、北半球では太陽は南寄りに昇り、南半球では太陽は北寄りに上ります。
問3-1
解答:エ
解説:
金星の動きと状態を把握するために用いる図は、選択肢エです。
選択肢エでは、金星は観察者の右側を西から東へ移動しているので、明けの明星です。
問3-2
解答:オ
解説:
火星は外惑星なので、選択肢オまたはカが該当します。
満ち欠けは、天体が公転して太陽の光の当たり方(光って見える範囲)が変わるために起こるので、選択肢オが適しています。
選択肢カでは、火星は地球に同じ面を向けているため、満ち欠けしません。
大問5 生物総合問題(進化・植物・血液循環)


問1
解答:ア
解説:
ア:正しい。
イ:相同器官の説明は正しいです。進化の起源は魚類で共通です。
ウ:進化とは、ある共通の祖先から長い年月をかけて枝分かれすることです。
エ:進化の説明なので、誤りです。
問2
解答:ア、ウ、キ
解説:
ア:無脊椎動物の特徴なので、正しい。
イ:昆虫類はあしは3対ありますが、同じ節足動物のクモ類はあしが4対あります。
ウ:正しい。
エ:軟体動物の特徴です。
オ:クラゲは刺胞動物です。
カ:タニシは軟体動物です。
キ:正しい。
問3
解答:エ
解説:
ア:コケ植物とシダ植物両方の特徴です。
イ:種子植物の特徴です。
ウ:被子植物の特徴です。
エ:正しい。
オ:コケ植物の特徴です。
問4-1
解答:ク
解説:
ペットボトルは胸腔、ゴム風船は肺胞、ゴム膜は横隔膜を表しています。
横隔膜が下がると胸腔内の気圧が下がり、肺が膨らんで肺に空気が入ります。
問4-2
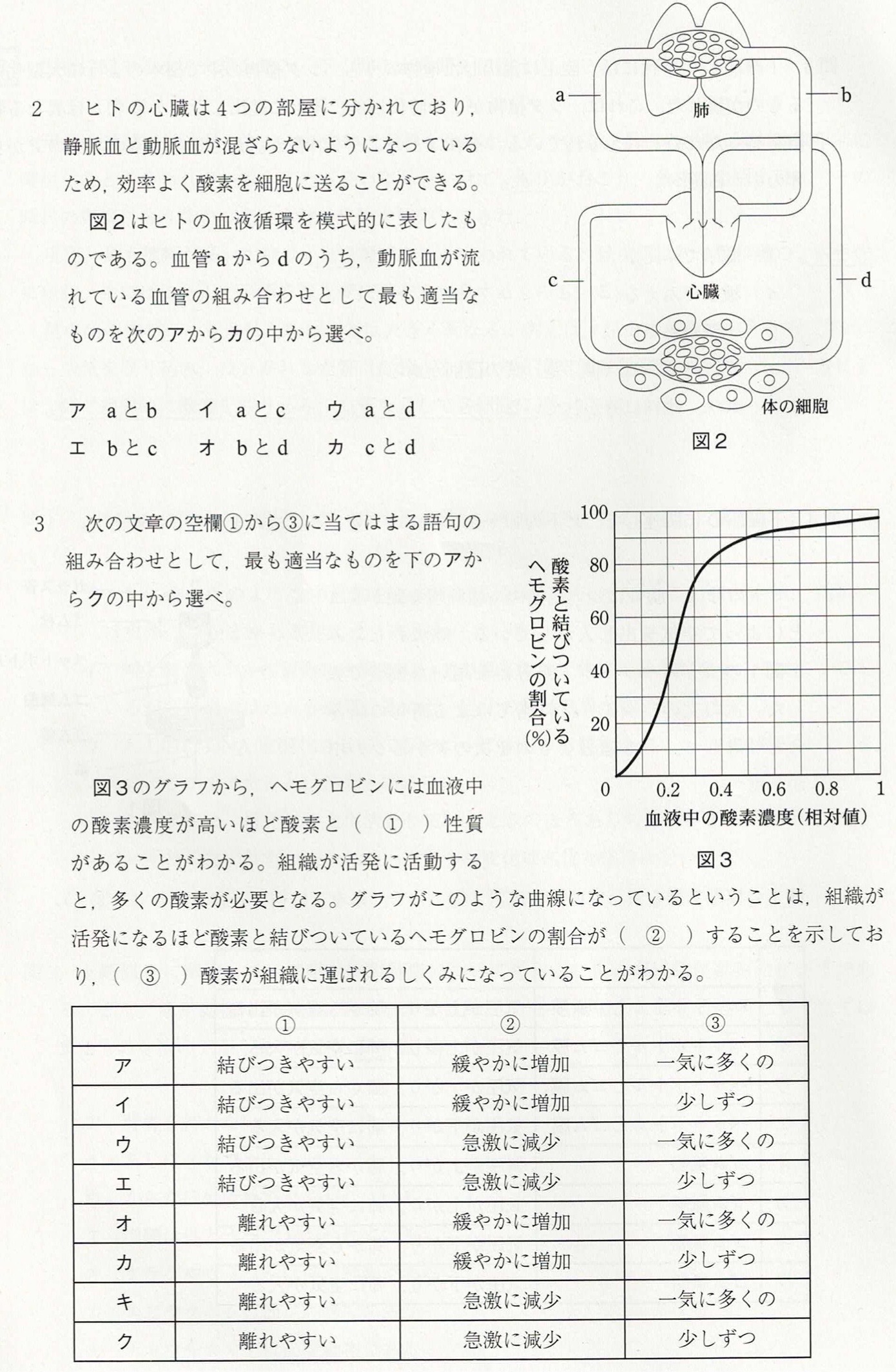
解答:オ
解説:
動脈血は肺でガス交換をした後の血液なので、bの肺静脈とdの大動脈が当てはまります。
問4-3
解答:ウ
解説:
①
グラフより、血液中の酸素濃度が高いほど、酸素と結びついているヘモグロビンの割合が高くなっているので、ヘモグロビンは酸素濃度が高いほど酸素と結びつきやすいことが分かります。
②
組織が活発になると血液中の酸素濃度は減少します。グラフより、血液中の酸素濃度が減少すると、酸素と結びついているヘモグロビンの割合が急激に減少することが分かります。
③
②の考察より、酸素濃度が減少すると、ヘモグロビンが酸素を一気に放出して組織に運ぶことが分かります。
大問6 総合問題(電池・刺激の伝達・養分の吸収など)



問1
解答:ウ
解説:
刺激の伝達経路は中枢神経から、中枢神経(大脳・脊髄)→運動神経→運動器官です。
問2
解答:①・・・〇、②・・・×、③・・・×、④・・・×
解説:
電池の成立要件は、電解質の水溶液を使用すること、異なる二種類の金属を使用することです。
①の食塩水は電解質の水溶液ですが、②〜③は非電解質なので水溶液中にイオンが無いため電流が流れません。
問3
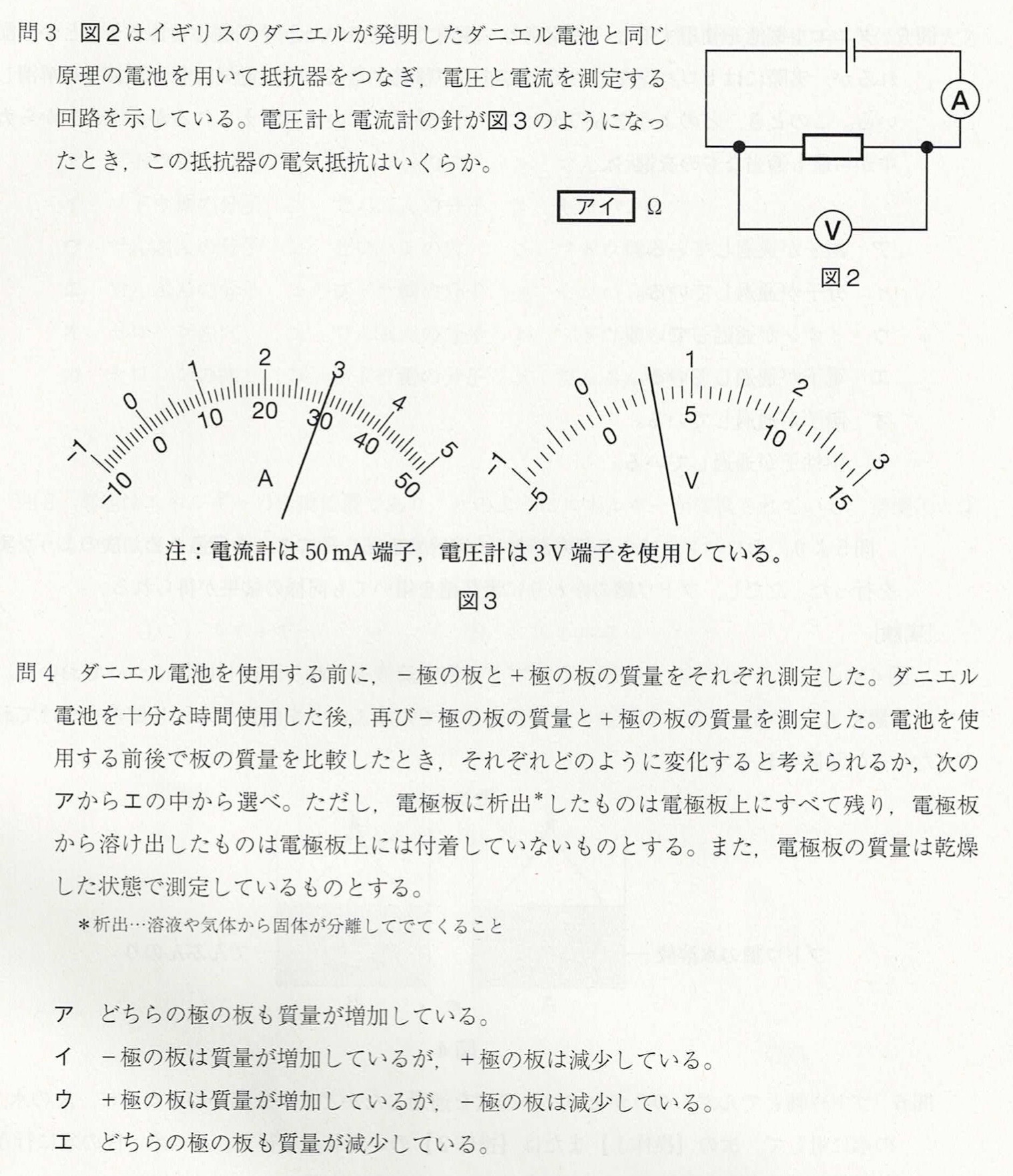
解答:ア・・・2、イ・・・0
解説:
オームの法則より、
R=V/I=0.6V÷30mA=0.6×1000÷30=600÷30=20Ω
問4
解答:ウ
解説:
亜鉛板(硫酸亜鉛水溶液)と銅板(硫酸銅水溶液)を使用した場合で考えます。
ア:亜鉛板(-極)は溶けているため、質量は減少しています。
イ:銅板(+極)上には硫酸銅水溶液が電子を受け取り銅が析出するため、質量が増加しています。
ウ:正しい
エ:選択肢アとイの考察より、誤りです。
問5
解答:ウ
解説:
亜鉛板側では亜鉛イオンが生じるため電気が+に傾き、銅板側では銅イオンが銅になるため電気が-に傾きます。
これらの電気の偏りをなくすために、セロハン膜を通じて、亜鉛イオンが銅板側へ、硫酸イオンが亜鉛板側へ移動します。
問6
解答:ウ
解説:
Aではブドウ糖やブドウ糖がいくつか結合したものを検出できるベネジクト液を使用します。
Bでは、デンプンを検出できるヨウ素液を使用します。
問7
解答:ウ
解説:
Aではベネジクト液が赤褐色に変化しますが、Bではヨウ素液の色は変化しないのが、一般的な結果です。
これより、Aではブドウ糖の分子がセロハンの穴を通過しますが、Bではデンプンの分子がセロハンの穴を通過しないことが分かります。
よって選択肢ウが正解です。
問8
解答:①・・・カ、②・・・オ
解説:
本問で用いている電池は、物質の化学エネルギーを電気エネルギーに変換する装置です。




