第1問

(1)(2)
マグネシウムと酸素は、3:2の質量比で化合します(定比例の法則)。
(3)
マグネシウムの燃焼の化学反応式は、
2Mg+O2→2MgO
これより、マグネシウム原子が12個反応すると、酸素分子は12/2=6個反応し、4個余ります。
(4)
燃焼により化合するマグネシウムと酸素の質量比は3:2より、酸化マグネシウムは5の質量比となります。
これより、過不足すべて反応したマグネシウムの質量は、4.5×3/5g=0.9×3=2.7g
(5)
①
質量保存の法則より、燃焼により化合した酸素の質量は、5.7-3.7=2.0g
②
燃焼により化合するマグネシウムと酸素の質量比は3:2より、酸素と化合したマグネシウムの質量は3.0gです。
③
3.7-3.0=0.7g
(6)
解答例:マグネシウムに酸素がよく触れるようにするため。(解説略)
第2問
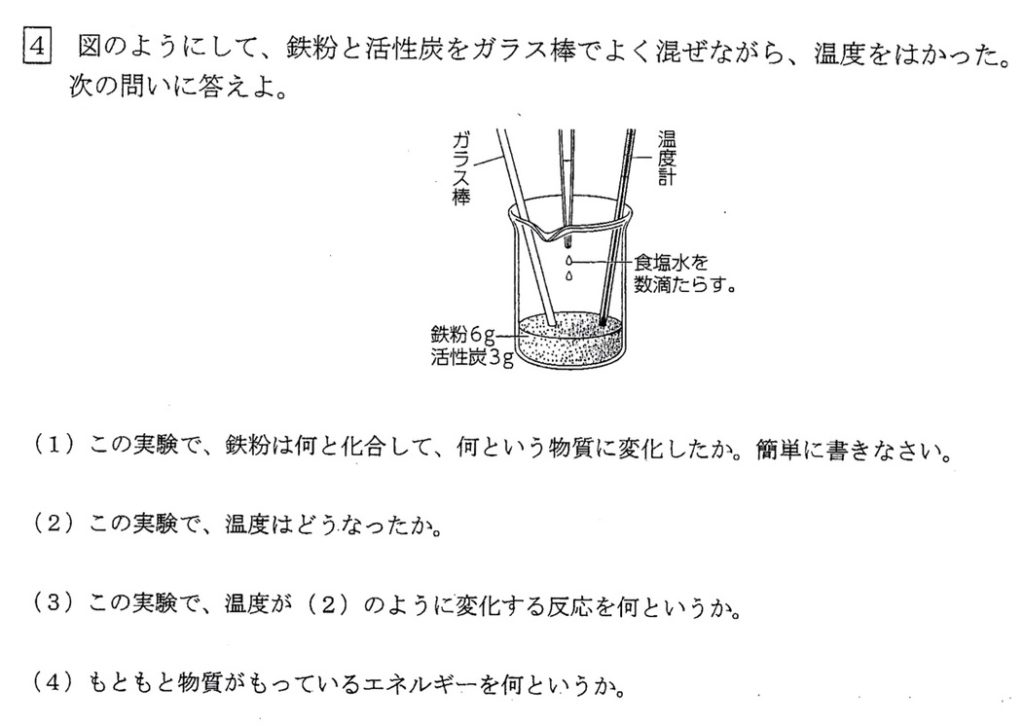
(1)
化学カイロでは、鉄は空気中の酸素と活性炭に吸着された水と反応して、水酸化鉄(Ⅲ)Fe(OH)3という酸化鉄ができます。
(2)(3)
化学カイロより、発熱反応によって周囲の温度が上がります。
(4)
化学カイロでは、物質がもつ化学エネルギーが熱エネルギーとして放出されます。
発生した水酸化鉄(Ⅲ)Fe(OH)3は、反応前より化学エネルギーの小さい別の物質です。
スポンサーリンク
第3問
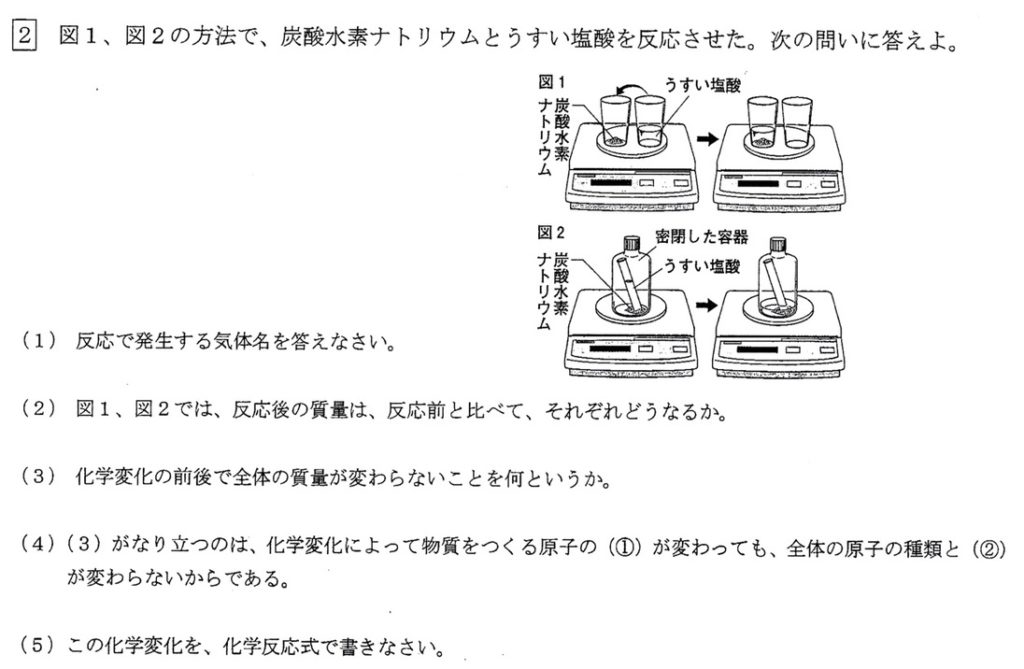
(1)
炭酸水素ナトリウムにうすい塩酸を加えると、塩化ナトリウム、水、二酸化炭素が発生します。
(2)(3)
図1は開放系より、発生した二酸化炭素の分だけ、反応前より質量が減少します。
図2は閉鎖系より、質量保存の法則より、反応前と反応後で質量は変化しません。
(4)
質量保存の法則が成り立つのは、物質をつくる原子の組み合わせが変わるが、原子の種類と数が変わらないからです。
(5)
NaHCO3+HCl→NaCl+H2O+CO2
第4問

(1)
カバーガラスを図のように、枝つき針を用いて端からゆっくりとかぶせるのは、気泡が入らないようにするためです。
(2)
解答例:ろ紙で吸い取る(解説略)
(3)
明るさを調節するのは、ステージ上下式顕微鏡の反射鏡です。
(4)
150/10=15倍
(5)
図2より、細胞壁と葉緑体が観察されたので、植物細胞だと推測できます。