第1問
(1)(2)(3)
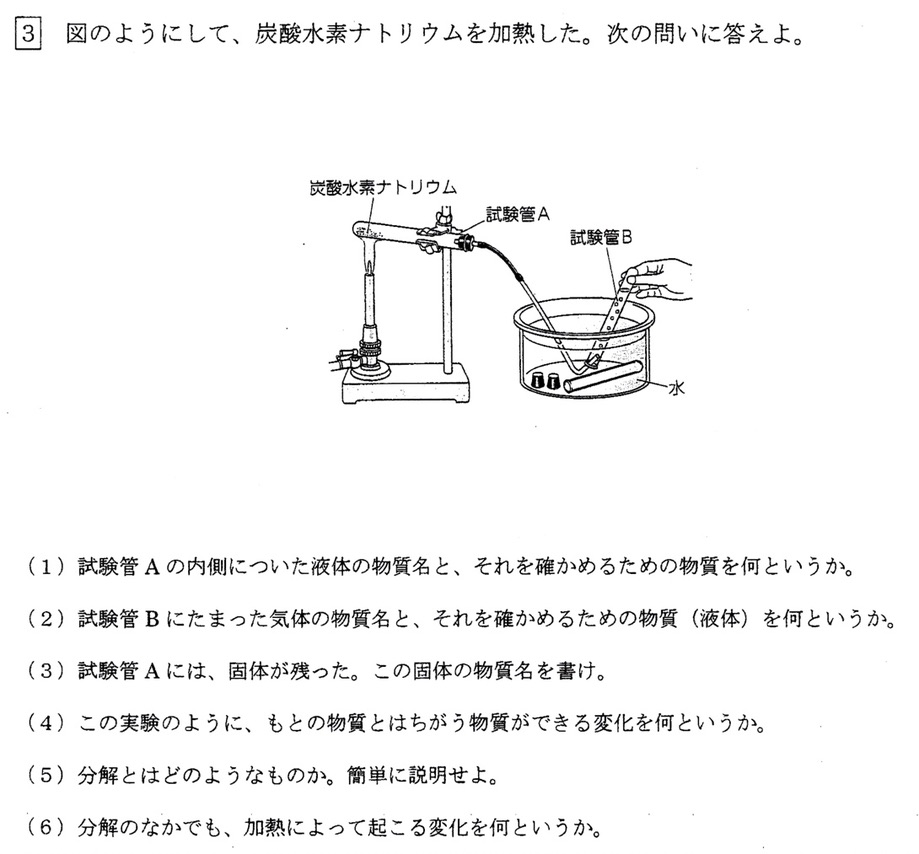
炭酸水素ナトリウムの熱分解により、固体として炭酸水素ナトリウムが、液体として水が、気体として二酸化炭素が発生します。
水の試薬として塩化コバルト紙があり、水につけると青色から赤色に変化します。
二酸化炭素を石灰水に通すと中和が起こり、水にとけにくい炭酸カルシウム(白色)の塩ができ、水溶液が白く濁ります。
このまま二酸化炭素を通し続けると、炭酸カルシウムが水に溶けやすい炭酸水素カルシウムになり、水溶液が再び透明になります。
(4)
物質の原子の組み合わせと数が変わり、違う物質になる変化を化学変化といいます。
(5)
分解とは、1種類の物質が2種類以上の別の物質に分かれることをいいます。
(6)
加熱によって起こる分解は熱分解です。
熱エネルギーを投入しているので、分解後の物質が持つエネルギーは、分解前の物質より高くなります。
第2問
(1)
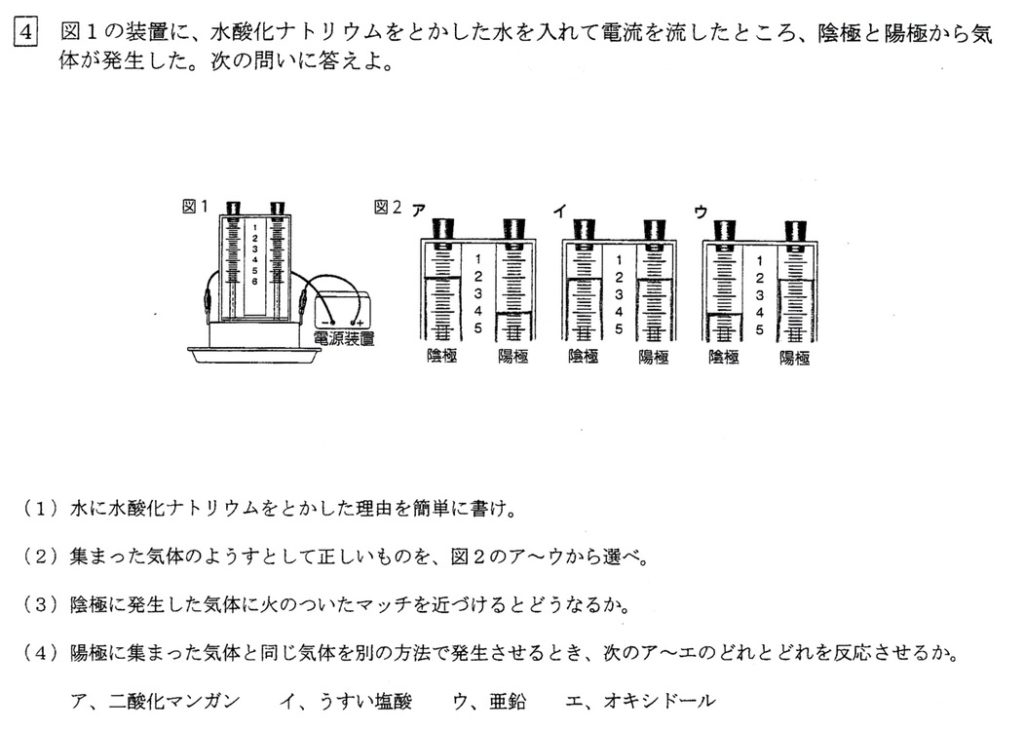
純粋な水は分子として存在しているため、電気を通しません。
そのため、電解質である水酸化ナトリウムを溶かすことで、電流が流れるようにします。
(2)
水酸化ナトリウム水溶液を電気すると水が電気分解され、陽極で酸素が、陰極で水素が発生します。
化学反応式は、
2H2O→2H2+O2
で、係数から、気体の体積比は、水素:酸素=2:1となり、ウが答えであることが分かります。
(3)
陰極では水素が発生し、マッチの火を近づけると「ポン」と音を立てて燃え、水が発生します。
(4)
陽極では気体の酸素が発生します。
酸素の発生法として、過酸化水素水(オキシドール)を二酸化マンガン(触媒)に通す方法があります。
亜鉛にうすい塩酸を加えると、塩化亜鉛と水素が発生します。
スポンサーリンク
第3問
(1)
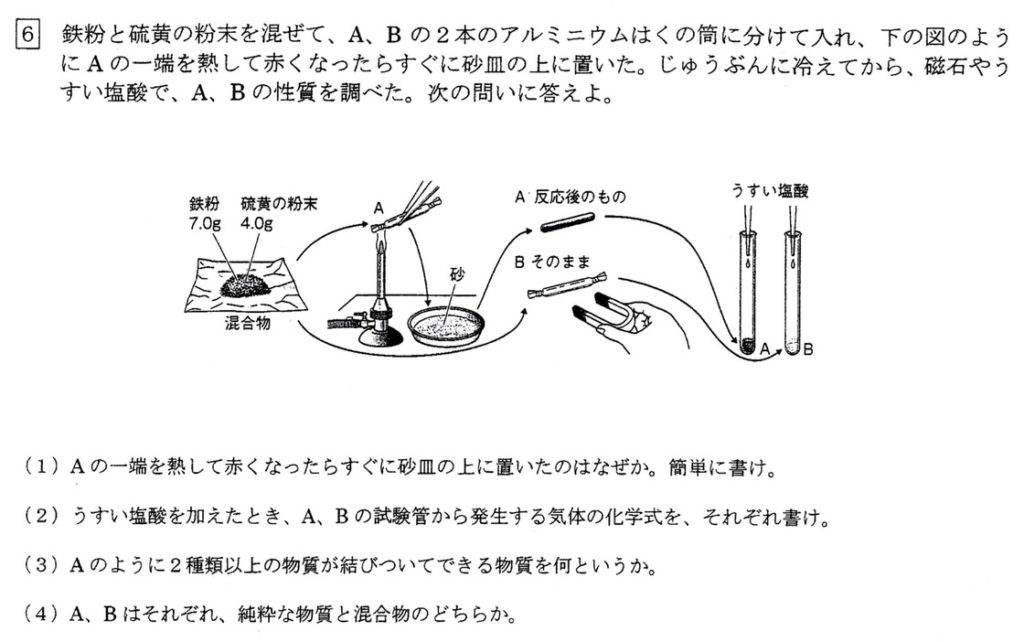
鉄と硫黄の化合は発熱反応より、反応が始まると、反応で発生した熱で反応が続きます。
(2)
・A
鉄と硫黄の化合により、黒色の硫化鉄が発生し、うすい塩酸を加えると卵に腐ったような臭いのする硫化水素(化学式:H2S)が発生します。
・B
鉄と硫黄の混合物より、うすい塩酸を加えると鉄が酸化され、水素(化学式:H2)が発生します。
(3)
答:化合物(解説略)
(4)
・A
硫化鉄のみ存在し、硫化鉄(FeS)は鉄(Fe)と硫黄(S)の化合物より、純粋な物質です。
・B
鉄と硫黄が混ざった粉末より、混合物です。
第4問
(1)(2)(3)
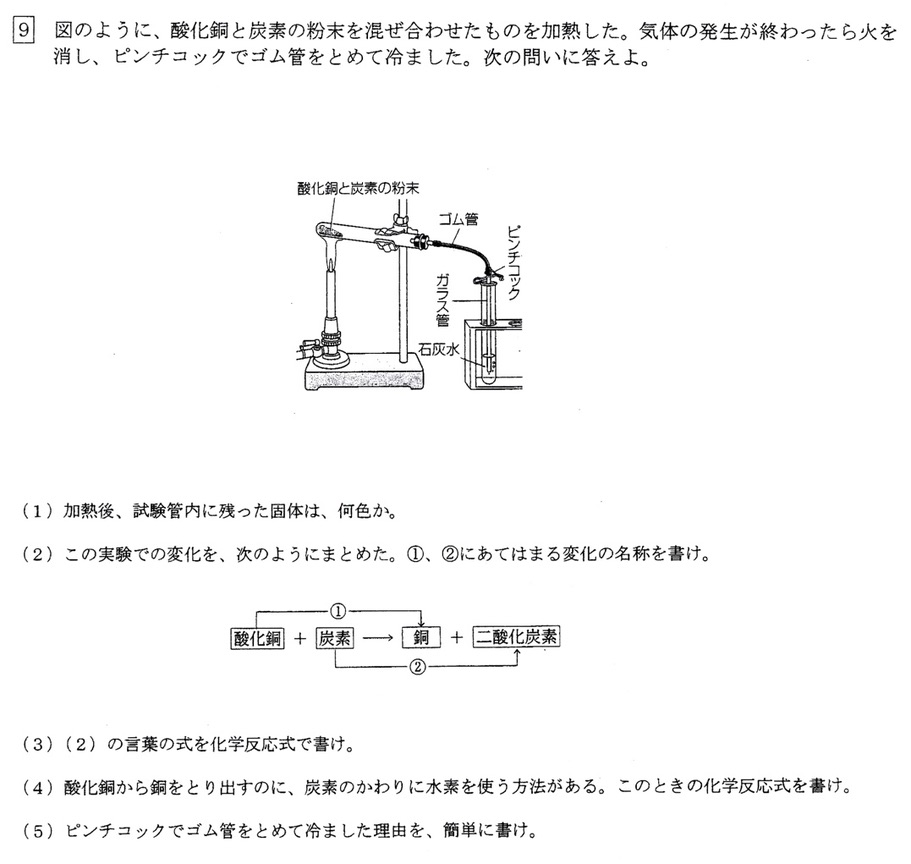
酸化銅の炭素による還元より、酸化銅は還元されて銅に、炭素は酸化されて二酸化炭素になります。
加えた炭素の量が酸化銅を全て還元するのに十分な量であるならば、反応後に残った固体は、全て銅(赤色)です。
化学反応式は、
2CuO+C→2Cu+CO2
です。
(4)
酸化銅の水素による還元の化学反応式は、以下の通りです。
CuO+H2→Cu+H2O
(5)
火を止めると試験管内の空気の温度が下がることで気圧が下がり、空気が試験管内に侵入してきます。
空気中には酸素が約21%含まれており、加熱された銅に触れることで酸化され、酸化銅に戻ってしまい、元の木阿弥となってしまいます。
それを防ぐために、問題文のような処理を施します。
よって答えは、空気中の酸素により銅が再び酸化銅となるのを防ぐため、です。