第1問
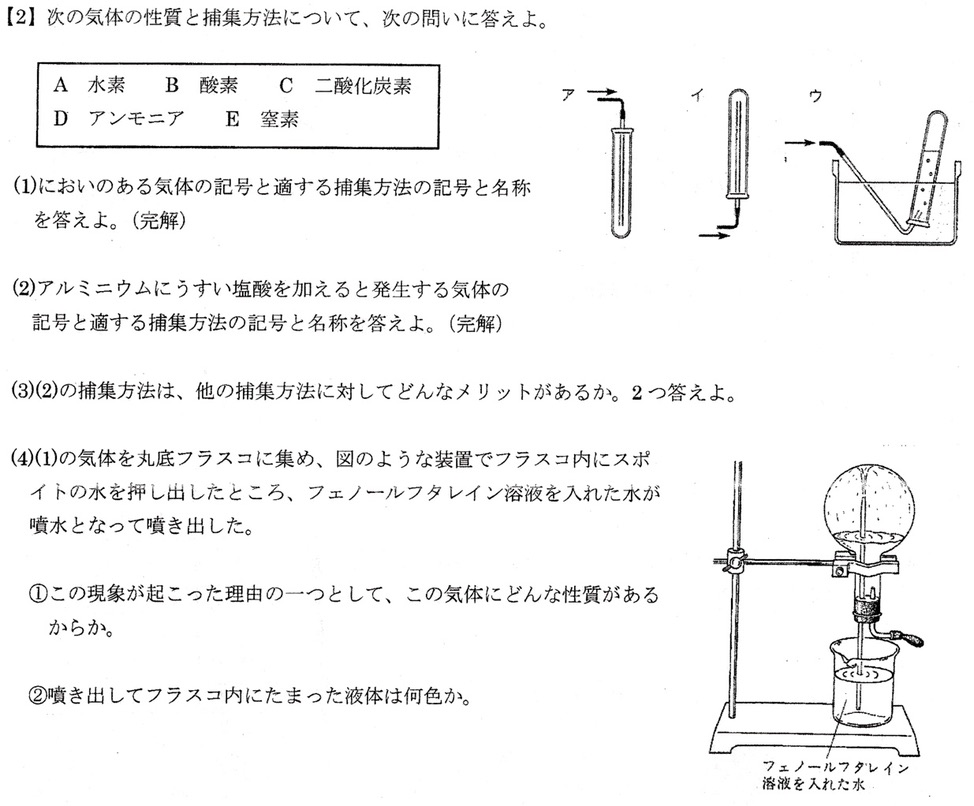
(1)
気体A〜Eの中でにおい(刺激臭)がある気体は、アンモニアです。
アンモニアは水に非常によく溶け(20℃の水1cm3に702cm3溶ける)、空気より軽い気体なので、上方置換法(イ)で捕集します。
(2)
アルミニウムは酸にもアルカリにも溶ける両性金属なので、うすい塩酸に溶けて水素が発生します。
水素は水に溶けにくく、最も軽い気体(空気の約0.07倍)より、水上置換法(ウ)で捕集するのが一般的です(上方置換法でも捕集できます)。
(3)
(2)の答えが水上置換法であった場合、たまる気体が目に見え、外気と触れないので他の気体と混ざらない、などのメリットが上げられます。
(4)
①
アンモニアは水に非常によく溶ける(20℃の水1cm3に702cm3溶ける)気体なので、スポイトから水を押し出すと、アンモニアが一気に溶けこみ、フラスコ内のアンモニアの気体分子が減少して気圧が急激に下がり、フラスコ内へ外気が取り込まれることで、水が勢いよく噴水のように流れ込みます。
②
アンモニアが水に溶けた水溶液はアルカリ性なので、フェノールフタレイン溶液の色が赤色に変化します。
第2問
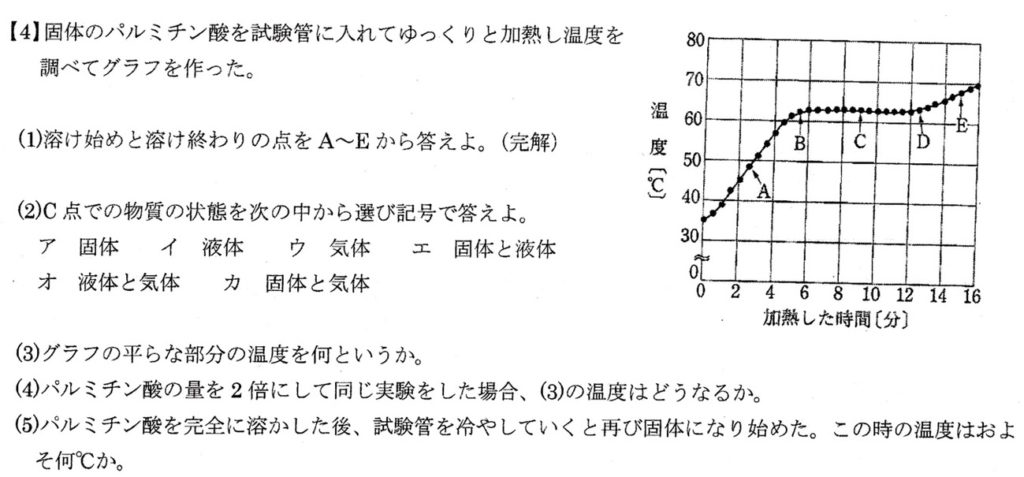
(1)
純粋なパルチミン酸の融点は62.7℃、沸点は360℃です。
状態変化のグラフでは、温度一定の状態が融点または沸点で、融点のときは固体と液体が併存しています。
よって、グラフでは溶け始めがB、溶け終わりがDです。
(2)
純粋なパルチミン酸の融点は62.7℃、沸点は360℃より、Cの温度では固体と液体が併存しています。
(3)
答:融点(解説略)
(4)
同一物質で量が増えると、融点と沸点は変化しませんが、温度一定の時間が長く、グラフの傾きが緩やかになります。
(5)
純粋なパルチミン酸の融点は62.7℃、沸点は360℃より、約63℃で固体になり始めます。
スポンサーリンク
第3問
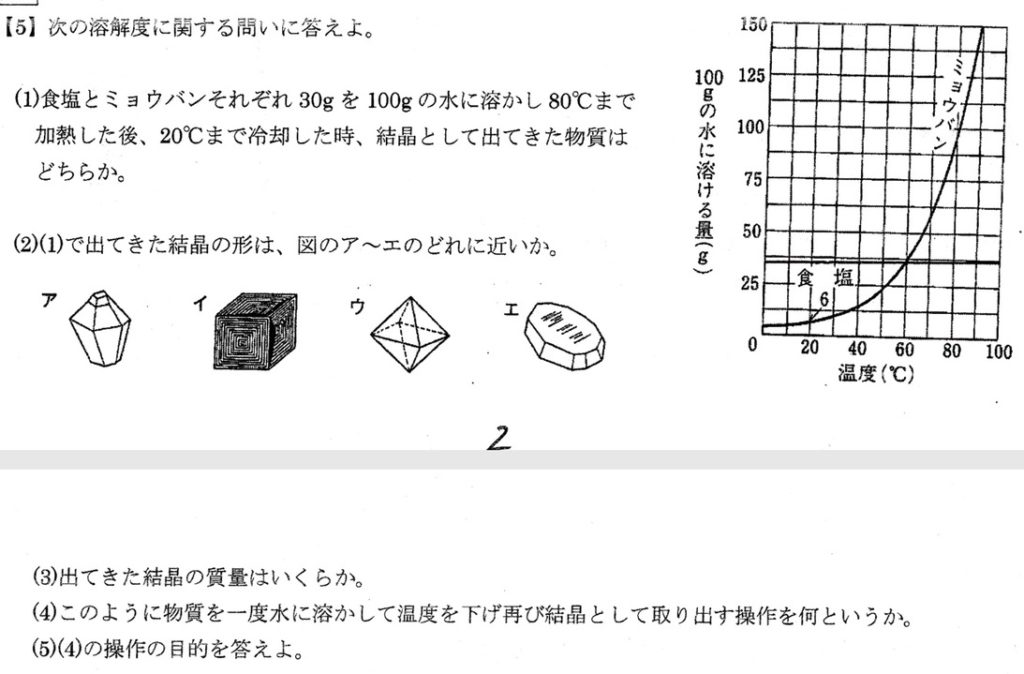
(1)
グラフより、80℃では塩化ナトリウム(食塩)とミョウバンは両方とも全て溶けていますが、20℃ではミョウバンの溶解度が6gと30g以下になるため、ミョウバンの結晶が析出します。
(2)
イは塩化ナトリウム、ウはミョウバン(答)、オはホウ酸の結晶です。
(3)
20℃におけるミョウバンの溶解度は6gより、30g – 6g=24gの結晶が析出します。
(4)
再結晶の方法の一つは、水溶液を冷やして取り出すです。
(5)
再結晶の目的は、混合物から不純物を取り除いて、純度の高い物質を取り出すことです。
第4問

(1)
解答例:突沸を防ぐため(解説略)
(2)
純粋なエタノールの沸点は78.3℃より、上記の温度がエタノールの沸点付近である試験管Aが、エタノールを最も多く含む混合物です。
(3)
エタノールはにおいのある引火性の物質なので、液体のにおいをかいだり、火を付けたりして、エタノールの有無を確認することができます。
(4)
蒸留は、物質の沸点の違いを利用して、液体の混合物を分ける(完璧には分離できない)方法です。
(5)
火を消すと枝つきフラスコ内部の温度が下がって内圧が下がり外気が取り込まれるので、試験管内部の液体が逆流するのを防ぐために、ガラス管の先を試験管から取り出してから火を消します。