栃木県公立高校入試オススメ過去問題集
★過去問

★模擬テスト
※模擬テストは1教科のみ表示。Amazonなどでは5教科すべて販売されています。
大問1 小問集合

1
解答:ウ
解説:
単純な知識問題なので、解説略。
2
解答:エ
解説:
単純な知識問題なので、解説略。
3
解答:イ
解説:
アとウとエは、加熱や冷却の仕組みを利用したものです。
4
解答:イ
解説:
20℃が融点より高く沸点より低い物質を選べばよいので、物質Bが正解です。
20℃では、物質Aの状態は気体、物質CとDの状態は固体です。
5
解答:受粉
解説:
単純な知識問題なので、解説略。
6
解答:乱反射
解説:
単純な知識問題なので、解説略。
7
解答:気団
解説:
単純な知識問題なので、解説略。
8
解答:中性子
解説:
単純な知識問題なので、解説略。
スポンサーリンク
大問2 火山岩のつくりとでき方


1
解答:ウ
解説:
顕微鏡の倍率=接眼レンズの倍率×対物レンズの倍率=10×2=20倍
岩石Xは深成岩でつくりは等粒状組織、岩石Yは火山岩でつくりは斑状組織です。
2
解答:イ
解説:
深成岩である花こう岩は、二酸化ケイ素含有量が多いため、白っぽい色をしています。
二酸化ケイ素含有量が多いと、セキエイやチョウ石などの無色透明の割合も多くなります。
3
解答:
斑晶・・・(例)地下深くで、ゆっくり冷え固まってできた。
石基・・・(例)地表付近で、急に冷え固まってできた。
解説:
ミョウバン水溶液実験のはなしをしています。
斑晶は表2より、ミョウバンの大きな結晶を表しています。この結晶はペトリ皿PとQに共通していることから、ゆっくり冷え固まってできたと言えます。また、観察(1)と(2)からは言えませんが、斑晶はマグマが地下深いところでゆっくり冷え固まってできたものです。
石基は表2より、ミョウバンの小さな結晶を表しています。この結晶はペトリ皿Qのみに現れていることから、急に冷えて固まってできたと言えます。また、観察(1)と(2)からは言えませんが、石基はマグマが地表や地表付近で急に冷え固まってできたものです。
スポンサーリンク
大問3 二酸化炭素の定量
1
解答:

解説:
炭酸水素ナトリウムに塩酸を加えると、気体として二酸化炭素(CO2)が発生します。
2
解答:
解説:
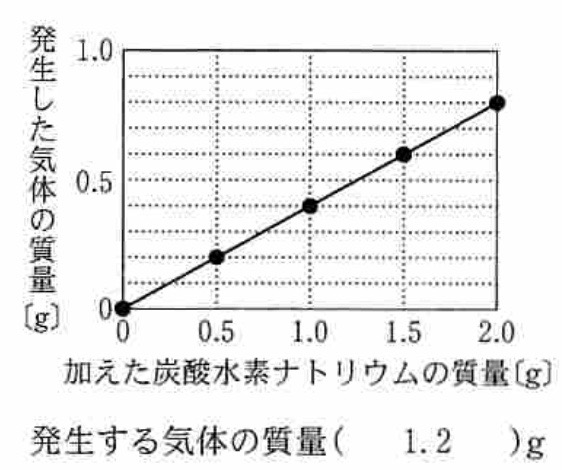
発生した二酸化炭素の質量=反応後にふたをゆるめた後の質量[g] – 反応後にふたをゆるめる前の質量[g]
上式に当てはめると、加えた炭酸水素ナトリウムの質量[g]を0.5gずつ増やしていくと、二酸化炭素の発生量が0.2gずつ増えていくことが分かるので、グラフが得られます。
この実験で用いたうすい塩酸25gが、炭酸水素ナトリウム3.0gを完全に反応させたと仮定します。表より、炭酸水素ナトリウム0.5gで二酸化炭素が0.2g発生することから、6倍して、炭酸水素ナトリウム3.0gで二酸化炭素が1.2g発生します。
3
解答:記号・・・X、理由・・・(例)塩酸の濃度を変えても、加える炭酸水素ナトリウムの質量が同じであるため、発生する気体の質量は変わらないから。
解説:
実験(1)〜(3)より、うすい塩酸25gを加えると、容器BからEの炭酸水素ナトリウムは完全に反応し、炭酸水素ナトリウムを0.5gずつ増やすと、二酸化炭素が0.2gずつ増えていきます。
ゆえに、塩酸の濃度を濃くしても、容器BからEの炭酸水素ナトリウムの質量が同じであるなら、発生する二酸化炭素の質量は変わりません。
加える炭酸水素ナトリウムの質量を増やしていくと、うすい塩酸の質量が一定であるため、発生する二酸化炭素の質量が一定になります。塩酸の濃度を濃くすると、一定の質量の塩酸と反応する炭酸水素ナトリウムの質量が増えるため、塩酸から発生する二酸化炭素の質量が増えます。
大問4 オームの法則
1
解答:120mA
解説:
図4より、−端子が500mAに接続されているので、100mA単位で目盛りを読みます。
2
解答:電圧・・・2V、電気抵抗・・・15Ω
解説:
直列回路なので、抵抗器Yに加わる電圧の大きさはオームの法則より、
V=IR=0.20A×10Ω=2.0V
回路全体の抵抗はオームの法則より、
R=V/I=5.0V/0.20A=50/2=25Ω
直列回路なので、抵抗器Zの抵抗は、25Ω-10Ω=15Ωです。
(別解)
抵抗器Zに加わる電圧の大きさが3.0V(5.0V-2.0V)、電流の大きさが0.20Aだから、抵抗の大きさはオームの法則より、
R=V/I=3.0V/0.20A=30/2=15Ω
3
解答:記号・・・エ、電流の大きさ・・・1.0A
解説:
回路全体の抵抗が小さくなるものを選びます。
ア:回路全体の抵抗は10Ωです。
イ:回路全体の抵抗は10Ω+10Ω=20Ωです。
ウ:回路全体の抵抗は、(10Ω×20Ω)/(10Ω+20Ω)=200/30=20/3≒6.7Ω
エ:回路全体の抵抗は、10Ω/2=5Ω
よって、選択肢エのスイッチAとCを閉じると、回路全体の抵抗が最も小さくなり、オームの法則より、回路全体の電流の大きさが最も大きくなります。
このときの電流の大きさは、オームの法則より、
I=V/R=5.0V/5Ω=1.0A
大問5 セキツイ動物と無セキツイ動物の分類


1
解答:ア
解説:
節足動物を選びます。
ア:正しい。
イ:イカは軟体動物です。
ウ:マイマイは軟体動物です。
エ:アサリは軟体動物です。
2
解答:①・・・えら、②・・・肺、③・・・皮膚
解説:
イモリは両生類なので、子はえら呼吸、親は主に肺呼吸をし、補助的に皮膚呼吸もします。
3
解答:①・・・食物連鎖、②・・・ウ
解説:
食物連鎖において、植物が生産者、ウサギが草食動物で一次消費者、キツネが肉食動物で二次消費者です。
肉食動物は、目が正面についているため視野が立体的に見え、獲物との距離感がつかめ、獲物を捕らえやすいです。
草食動物は、目が側面についているため視野が広く、敵を見つけて逃げやすいです。
大問6 中和とイオン数 ★3がやや難

1
解答:ア
解説:
塩酸は酸性の水溶液なので、BTB溶液の色は、緑色→黄色になります。
塩酸は気体の塩化水素が水に溶けた水溶液です。
溶けるということはイオンに電離するということで、塩化水素は以下のように電離して塩酸になります。
HCl → H+ + Cl–
水素イオンが生じていることから、塩酸は酸性の水溶液です。
2
解答:(例)水溶液の水を蒸発させる。
解説:
塩酸と水酸化ナトリウムの反応により中和が起こります。化学反応式は、以下のとおりです。
HCl+NaOH→NaCl+H2O
中和により塩として塩化ナトリウム(塩)が生じます。塩化ナトリウムは水にとけて電離しており、沈殿は生じません。
塩化ナトリウムは温度による溶解度の変化が少ないので、水溶液を加熱して水を蒸発させる方法を取ります。
3 ★やや難
解答:
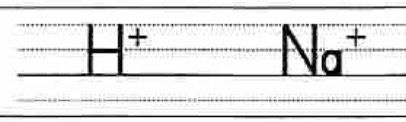
解説:
塩酸と水酸化ナトリウムの中和に関係する、化学反応式と電離式を書いて考えます。
HCl+NaOH→NaCl+H2O
HCl → H+ + Cl–
NaOH → Na+ + OH–
H+ + OH– → H2O
Na+ + Cl– → NaCl
これより、水酸化ナトリウム水溶液を1回加えると、H+が1個減って、Na+が1個増えるので、直線の傾きどうしの積が-1となり、2直線が垂直に交わります。
H+の直線とNa+の直線とy軸(イオン数)で直角二等辺三角形ができるので、2直線の交点におけるイオン数は等しくなります。
4
解答:エ
解説:
塩酸と水酸化ナトリウムの中和に関係する、化学反応式と電離式を書いて考えます。
HCl+NaOH→NaCl+H2O
HCl → H+ + Cl–
NaOH → Na+ + OH–
H+ + OH– → H2O
Na+ + Cl– → NaCl
中和が起こると、H+とOH–が1個ずつ減りますが、Na+とCl–が1個ずつ加わるため、全体のイオン数は変化しません。
しかし中和が起こらなくなると、NaOHを1回加えると、Na+とOH–が1個ずつ加わるため、全体のイオン数は2個ずつ増えていきます。
以上より、答えは選択肢エです。
大問7 太陽の高度の測定

1
解答:日周運動
解説:
地球は地軸の北極側から見て、西から東に1日360°(1時間で15°)自転するため、太陽は東から西へ動いて見えます。これを、日周運動といいます。
太陽は1時間で15°東から西へ動いて見えるので、日影は1時間で15°西から東へ動いていきます。
2
解答:①・・・Q、②・・・S
解説:
太陽は1時間で15°東から西へ動いて見えるので、日影は1時間で15°西から東へ動いていきます。
秋分の日(9/20頃)から3か月後は、冬至の日(12/20頃)です。
天球上において冬至の日の太陽の動きは、南寄りの東から登り、南寄りの西に沈むので、日影は北よりの西から始まり、北よりの東へ動いていきます。
3
解答:ア、イ
解説:
棒の長さと影の長さが等しくなるためには、太陽の南中高度が45°になる必要があります。
太陽の南中高度は、
・春分と秋分:90°-緯度
・夏至:90°-緯度+23.4°
・冬至:90°-緯度-23.4°
地点Xの緯度は北緯37°であるので、太陽の南中高度が45°になるのは、秋分から冬至、または冬至から秋分の間であると考えられます。
4
解答:①・・・53度、②・・・22度、③・・・地点Y
解説:
①
地点Xの緯度は北緯37°、秋分の日の太陽の南中高度は90°-緯度であるので、南中高度=90°-37°=53°
②
水平な地面とのなす角度が15°のとき、ソーラーパネルと太陽とのなす角度は、53°+15°=68°です。
問題文に「ソーラーパネルの発電効率が最も高くなるのは、太陽光の当たる角度が垂直のとき」とあるので、
ソーラーパネルと太陽とのなす角度が、53°+15°+22°=90°であればよいです。
よって、15°からさらに22°大きくする必要があります。
③
地点Yの緯度は北緯40°、秋分の日の太陽の南中高度は90°-緯度であるので、南中高度=90°-40°=50°
ソーラーパネルの発電効率が最も高くなるためには、ソーラーパネルと太陽とのなす角度が、50°+15°+25°=90°であればよいです。
ソーラーパネルの発電効率が最も高くなる角度は、地点Xが15°+22°=37°、地点Yが15°+25°=40°より、地点Yの方が角度が大きくなります。
これらの考察から、ソーラーパネルの発電効率が最も高くなる角度は、ともにその地点の緯度と等しくなることが分かります。
大問8 光合成量と呼吸量の計算

1
解答:ウ
解説:
あたためたエタノールに入れるのは、葉の緑色を脱色してヨウ素液の色の変化を見やすくするためです。
2
解答:デンプン
解説:
袋Aでは葉に強い光が当たっており、ヨウ素液の色が青紫色に変化したことから、光合成によってデンプンが作られたことが分かります。
3
解答:ア
解説:
袋A:葉+二酸化炭素+光→光合成によりデンプンが生じた
袋C:葉+二酸化炭素→デンプンは生じなかった
袋Aと袋Cの比較(対照実験)から、光合成には光が必要であることが分かります。
4
解答:(例)光合成によって吸収された二酸化炭素の量と、呼吸によって放出された二酸化炭素の量がつり合っているから。
解説:
袋A:葉+二酸化炭素+光→光合成により二酸化炭素が消費された
袋C:葉+二酸化炭素→袋Aとの比較より呼吸により二酸化炭素が増加した
袋E:葉+二酸化炭素+光→袋Aとの比較より、光合成により二酸化炭素が消費されるが、二酸化炭素量が変化しなかった。
袋Aと袋Eは条件が同じなのに、袋Eは二酸化炭素量が変化しなかったのは、光合成量と呼吸量がつり合っているからです。
つまり、光合成で消費される二酸化炭素量と、呼吸で消費される二酸化炭素量が等しいからです。
大問9 等速直線運動と等加速度運動 ★3と4がやや難
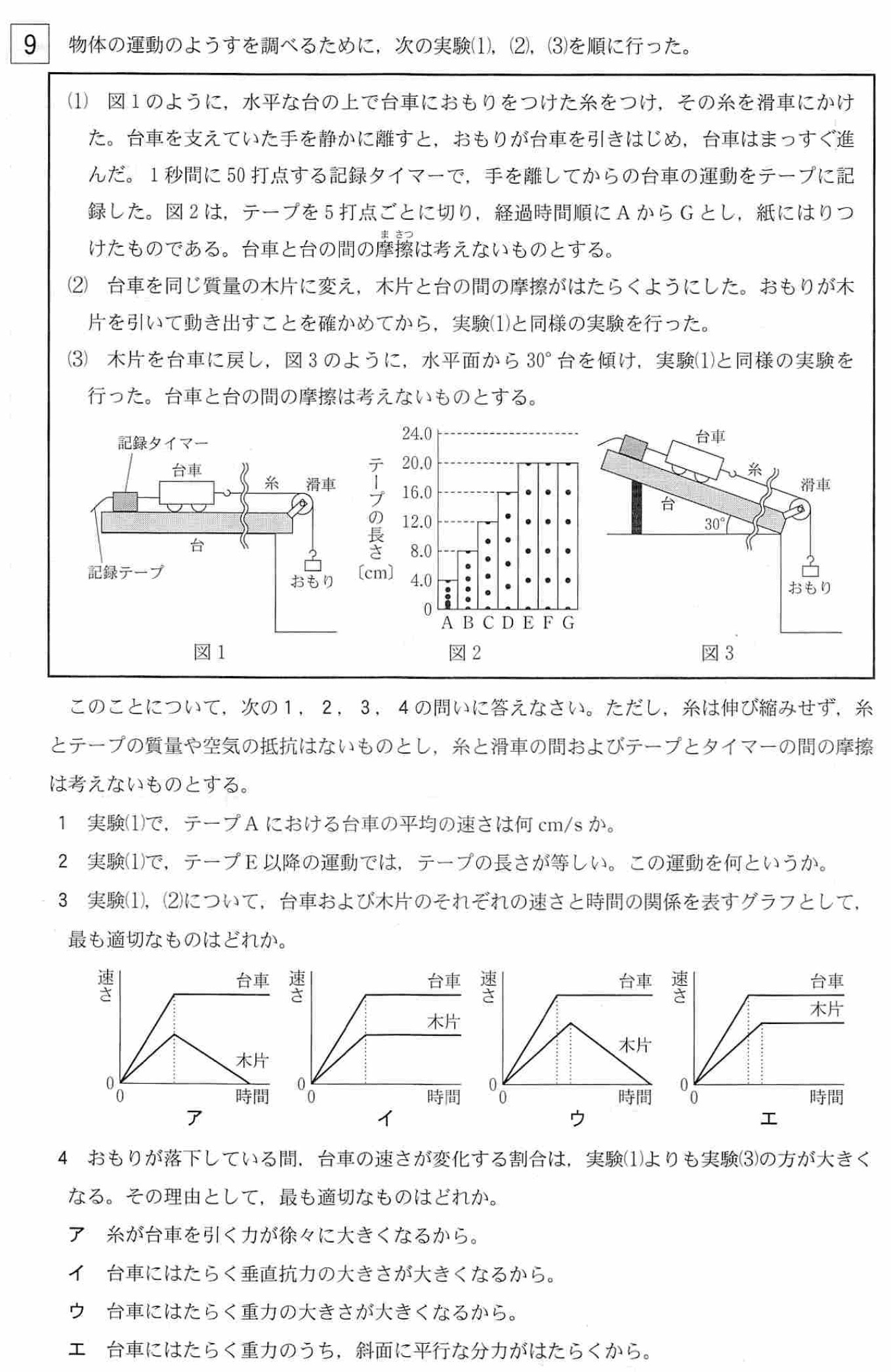
1
解答:40cm/s
解説:
1秒間に50打点するので、0.1秒で5打点します。
図2のテープAは、5打点(0.1秒)で4.0cmであるので、
平均の速さ=4.0cm/0.1s=40cm/s
2
解答:等速直線運動
解説:
図2のテープE、F、Gは、テープの長さが20.0cmと等しいから、平均の速さも20cm/0.1s=200cm/sと等しいので、等速直線運動をしていることが分かります。
3 ★やや難
解答:ウ
解説:
問題文に「おもりが木片を引いて動き出す」とあるので、糸が木片を引く力が木片にはたらく摩擦力(動摩擦力)よりも大きいと言え、木片は等加速度運動をしていることが分かります。
図2ではEの時点でおもりが床についたため、水平方向では台車に力が生じず、台車は等速直線運動をしています。
木片の場合、摩擦力(動摩擦力)が生じているために、おもりが床につく時間は、台車のときよりも遅くなります。
木片もおもりが床についた段階で、水平方向では木片には摩擦力が生じるため、木片は速さが一定の割合で減っていく、等加速度運動をします。
以上より、答えは選択肢ウです。
4 ★やや難
解答:エ
解説:
運動方程式より、加速度は台車の移動方向にはたらく力の大きさに比例し、台車の質量に反比例します。
実験(1)と(3)で、台車の質量は同じであるので、台車の移動方向にはたらく力の大きさのみ考えます。
実験(1)では、台車には、糸が台車を引く力(=おもりにはたらく重力の大きさ)が働きます。
実験(3)では、台車には、糸が台車を引く力(=おもりにはたらく重力の大きさ)と、台車にはたらく重力の斜面方向の分力(角度30°より、台車にはたらく重力×1/2)の2つが働きます。
よって、台車の移動方向にはたらく力の大きさは、実験(3)の方が台車にはたらく重力の斜面方向の分力だけ大きいので、台車の速さの変化する割合は、実験(3)の方が大きくなります。

