
👉教師紹介・料金
※授業料1回1,500円+交通費(コミコミ最大3,000円)・入会金なし・お好きな日時に受講・3回のお試し期間あり(無料教材あり)
☆学力テストはこれで完璧!オリジナル教材☆
👉北海道学力テストはこれで完璧!オリジナル教材+過去問一覧
※過去問の販売はできませんのでご注意ください。
中学3年北海道学力テスト第8回「理科」(2022年度)問題・解答・解説
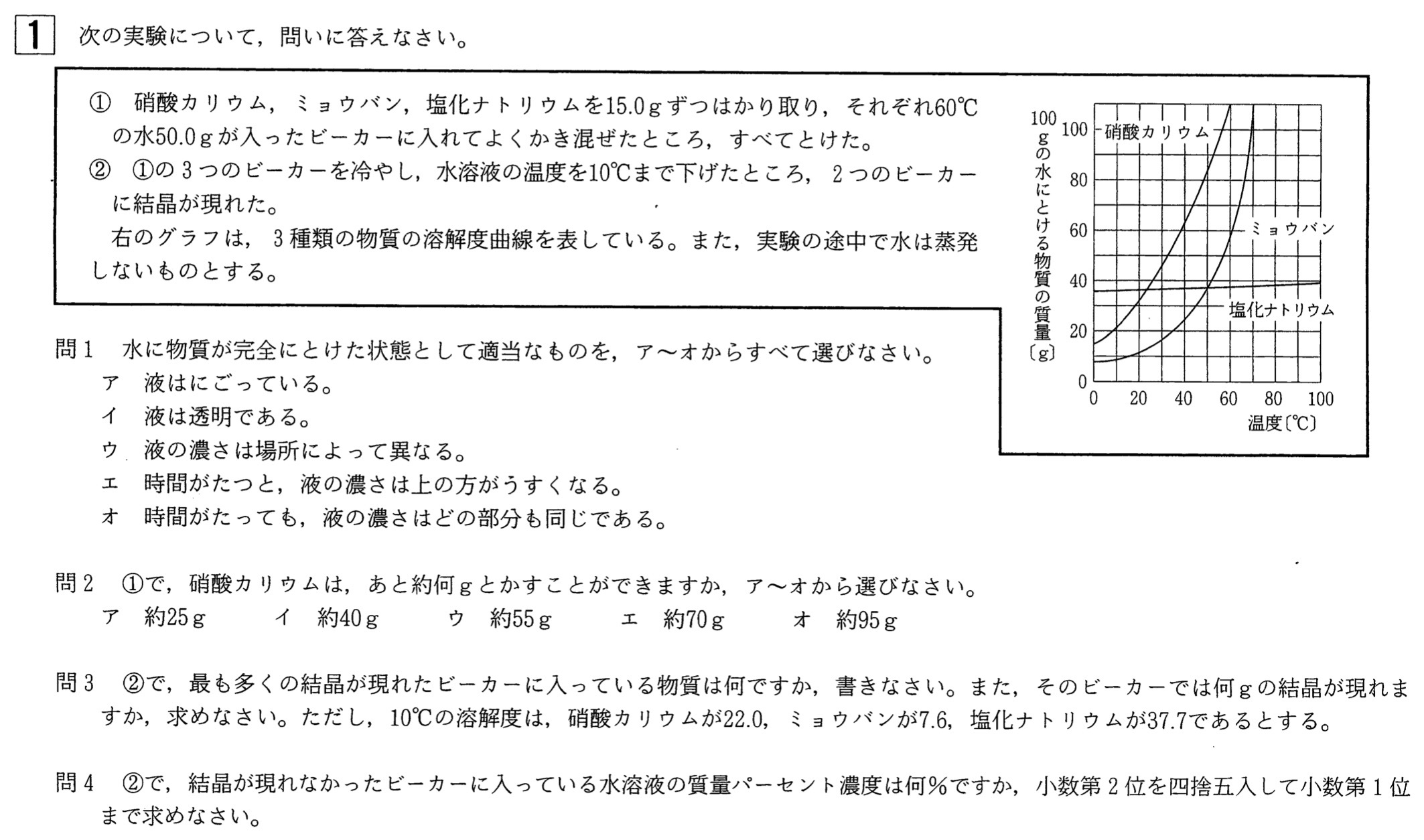
大問1 溶解度 ★問3と問4がやや難
問1
解答:イ、オ
解説:
おそらく水溶液の性質について問われているかと思いますが、「水に物質が完全にとけた状態」だけでは、解答できません。
が、問題文で使われている溶質が硝酸カリウム、ミョウバン、塩化ナトリウムなので、これら3つの溶媒が溶媒である水に完全にとけた状態が問われていると仮定して解答します。
ア:硝酸カリウム、ミョウバン、塩化ナトリウム、ともに水に完全に溶けると無色透明な水溶液になります。塩化銅が水に完全に溶けた水溶液では、水溶液の色は銅イオンのために青色になります。
イ:正しい。
ウ:水溶液中では、粒子は水分子と衝突して均一に散らばっているので、どの部分でも濃度は同じです。
エ:選択肢ウの考察より、誤りです。
オ:選択肢ウの考察より、正しい。
問2
解答:イ
解説:
溶解度曲線より、硝酸カリウムの溶解度(100gの水に溶けることができる限界の質量)は60℃では110gなので、60℃・50.0gの水には110g÷2=55g溶けることができます。
実験①より、60℃・50.0gの水に硝酸カリウムは15.0g溶けているので、あと55g-15g=40g溶けることができます。
問3 ★やや難
解答:物質・・・ミョウバン、結晶・・・11.2(g)
解説:
与えられた溶解度曲線より、塩化ナトリウムは温度を下げても溶解度はあまり変化しないので、冷やすことでの再結晶法では、析出量は最も少なくなります。
よって、硝酸カリウムかミョウバンのいずれかが答えになると考えられます。
実験①では60℃・50.0gの水に、硝酸カリウムとミョウバンをそれぞれ15.0g溶かしているので、溶解度曲線に合わせて、60℃・100gの水に、硝酸カリウムとミョウバンをそれぞれ15.0g×2=30.0g溶かしたと考えます。
与えられた溶解度曲線より、温度を60℃から10℃に下げると、ミョウバンの溶解度は60gから7.6gに、硝酸カリウムの溶解度は110gから22.0gに下がるので、結晶の析出量は、ミョウバンが30.0g-7.6g=22.4g、硝酸カリウムが30.0g-22.0g=8.0gです。
よって、ミョウバンの結晶が最も多く現れます。
また、これらの値は100gの水での析出量で、実験では50.0gの水を用いているので、実際の結晶の析出量は、ミョウバンが22.4g÷2=11.2g、硝酸カリウムが8.0g÷2=4.0gです。
問4 ★やや難
解答:23.1%
解説:
問3の考察より、塩化ナトリウムは結晶が析出しなかったと考えられますが、裏を取ります。
実験①では60℃・50.0gの水に、塩化ナトリウムを15.0g溶かしているので、溶解度曲線に合わせて、60℃・100gの水に、塩化ナトリウムを15.0g×2=30.0g溶かしたと考えます。
与えられた溶解度曲線より、温度を60℃から10℃に下げると、塩化ナトリウムの溶解度は37.7gと30.0gより少ないので、塩化ナトリウムの結晶は析出しません。
質量パーセント濃度は比なので、50.0gの水ではなく、100gの水に30.0gの塩化ナトリウムが溶けていると考えて計算します。
30.0g÷(100g+30.0g)×100=30/130×100=300/13=23.076・・・≒23.1%
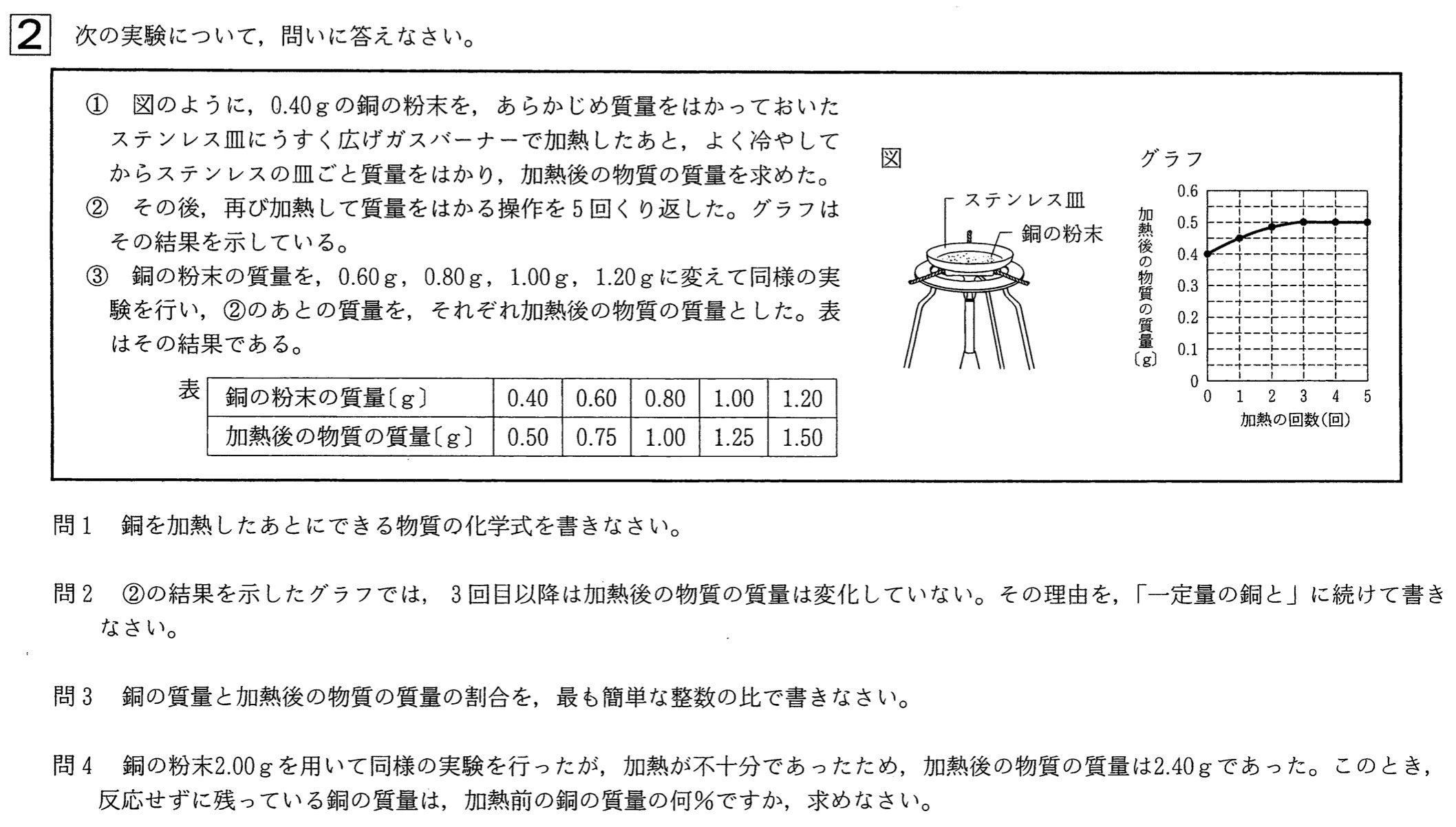
大問2 銅の酸化
問1
解答:CuO
解説:
単純な知識問題なので、解説略。
問2
解答:(一定量の銅と)結びつく酸素の質量に限界があるから。(例)
解説:
表より、質量比は、Cu:O2:CuO=0.40g:0.50g-0.40g:0.50g=4:1:5で一定の値を取るので、一定量の銅と化合する酸素の質量は一定であるので、グラフのように加熱を繰り返すと質量は増加しなくなります。
問3
解答:(銅:加熱後の物質=)4:5
解説:
問2解説参照。
問4
解答:20(%)
解説:
酸素は2.40g-2.00g=0.40g化合しています。
問2の考察より、質量比は、Cu:O2:CuO=4:1:5=1.60g:0.40g:2.00gです。
よって、反応した銅の質量は1.60gなので、未反応の銅の質量は2.00g-1.60g=0.40gです。
反応せずに残っている銅の質量と加熱前の銅の質量比は、0.40g/2.00g×100=1/5×100=20%
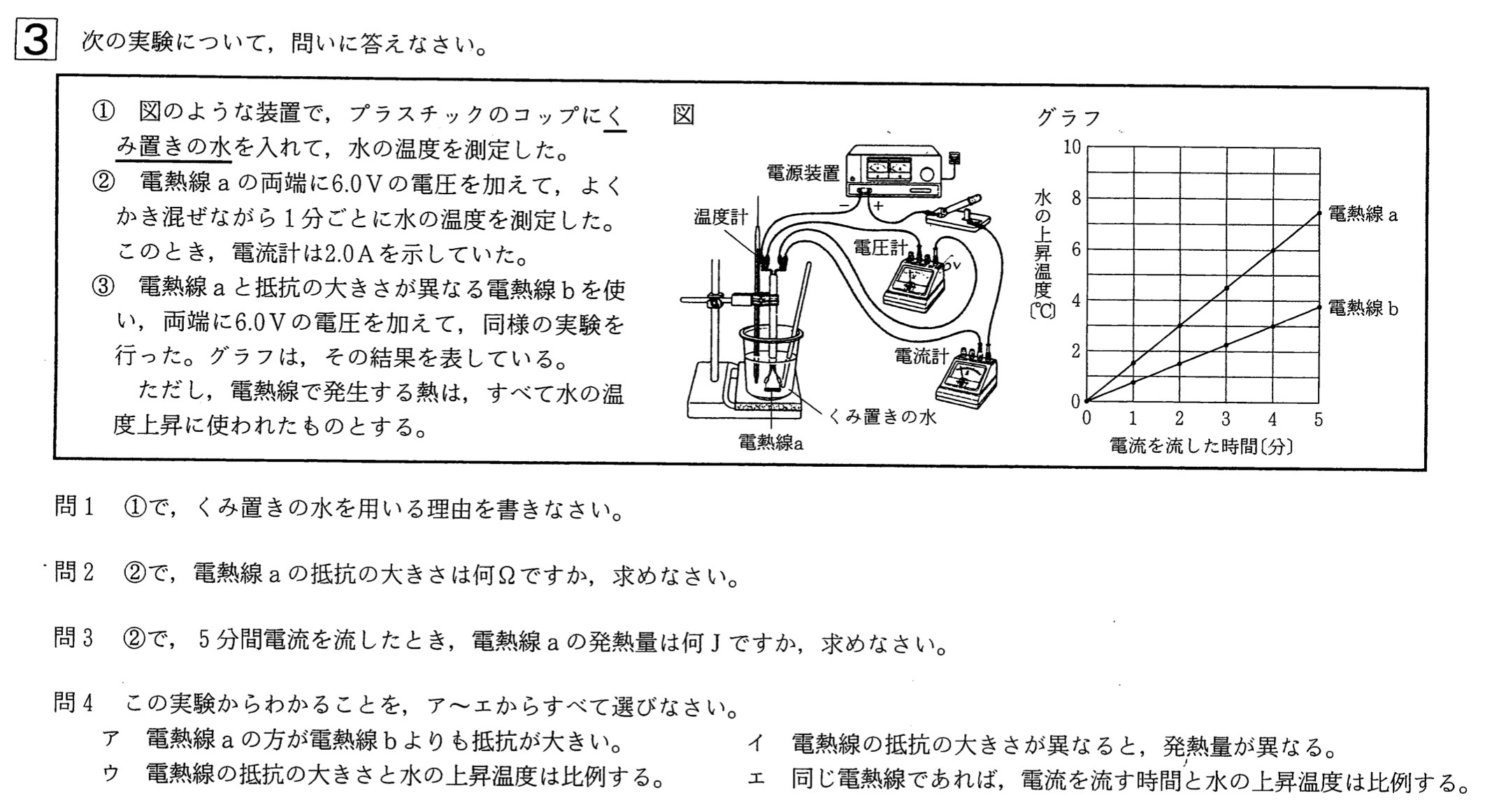
大問3 発熱量と上昇温度 ★問4が難
問1
解答:室温で水の温度が変化しないようにするため。(例)
解説:
単純な知識問題なので、解説略。
問2
解答:3.0Ω
解説:
実験②から、電熱線aに加わる電圧の大きさは6.0V、流れる電流の大きさは2.0Aより、オームの法則を用いて電熱線a抵抗の大きさを求めると、
V=IR⇔R=V/I=6.0V/2.0A=3.0Ω
問3
解答:3600(J)
解説:
熱の問題では、電熱線aで消費した電気エネルギーが全て熱エネルギーに変換された、という前提で考えます。
電熱線aの発熱量[J]=電熱線aで消費した電気エネルギー[J]=IVt=2.0A×6.0V×(5×60s)=60×60=3600J
問4 ★難
解答:イ、エ
解説:
問題文に「電熱線で発生する熱は、すべて水の温度上昇に使われたものとする。」と仮定されていることに留意して下さい。
・ア:
グラフより、電熱線bの方が電熱線aより水の上昇温度が低いので、以下の不等式が成り立ちます。
電熱線bの発熱により水が得た熱エネルギー[J]<電熱線aの発熱により水が得た熱エネルギー[J]
仮定より、
水が得た熱エネルギー[J]=電熱線の発熱量[J]=電熱線で消費した電気エネルギー[J]=IVt
実験②と③より、電熱線に加える電圧の大きさは6.0Vで一定なので、オームの法則を用いて以下の式で考えます。
水が得た熱エネルギー[J]=IVt=V2t/R
電熱線aの抵抗をRa、電熱線bの抵抗をRbと置くと、
V2t/Rb<V2t/Ra ⇔ 1/Rb<1/Ra ⇔ Ra<Rb
よって、電熱線bの方が電熱線aよりも抵抗が大きいです。
・イ:グラフより電熱線aと電熱線bで発熱量が異なっているので、正しい。
・ウ:
1gの水を1℃上昇させるのに必要な熱エネルギーを4.2Jと仮定すると、以下の式が成り立ちます。
水が得た熱エネルギー[J]=4.2[J/℃・g]×上昇温度[℃]×水の質量[g]
選択肢アの考察より、水が得た熱エネルギー[J]=IVt=V2t/R、であるので、
4.2[J/℃・g]×上昇温度[℃]×水の質量[g]=V2t/R
水の質量と電圧の大きさと電流を流す時間は同じであるので、
上昇温度[℃]=(V2t/4.2×水の質量)/R
となり、(V2t/4.2×水の質量)は定数と見なせるので、電熱線の抵抗の大きさと水の上昇温度は反比例します。
・エ:
選択肢アの考察より、水が得た熱エネルギー[J]=IVt=V2t/R=(V2/R)×t、選択肢ウの考察より、
4.2[J/℃・g]×上昇温度[℃]×水の質量[g]=(V2/R)×t ⇔ 上昇温度[℃]=(V2/R×4.2×水の質量)×t
これより、同じ電熱線すなわち抵抗の大きさが変わらず、加える電圧の大きさ・水の質量が変わらない場合、上昇温度は電流を流す時間に比例します。
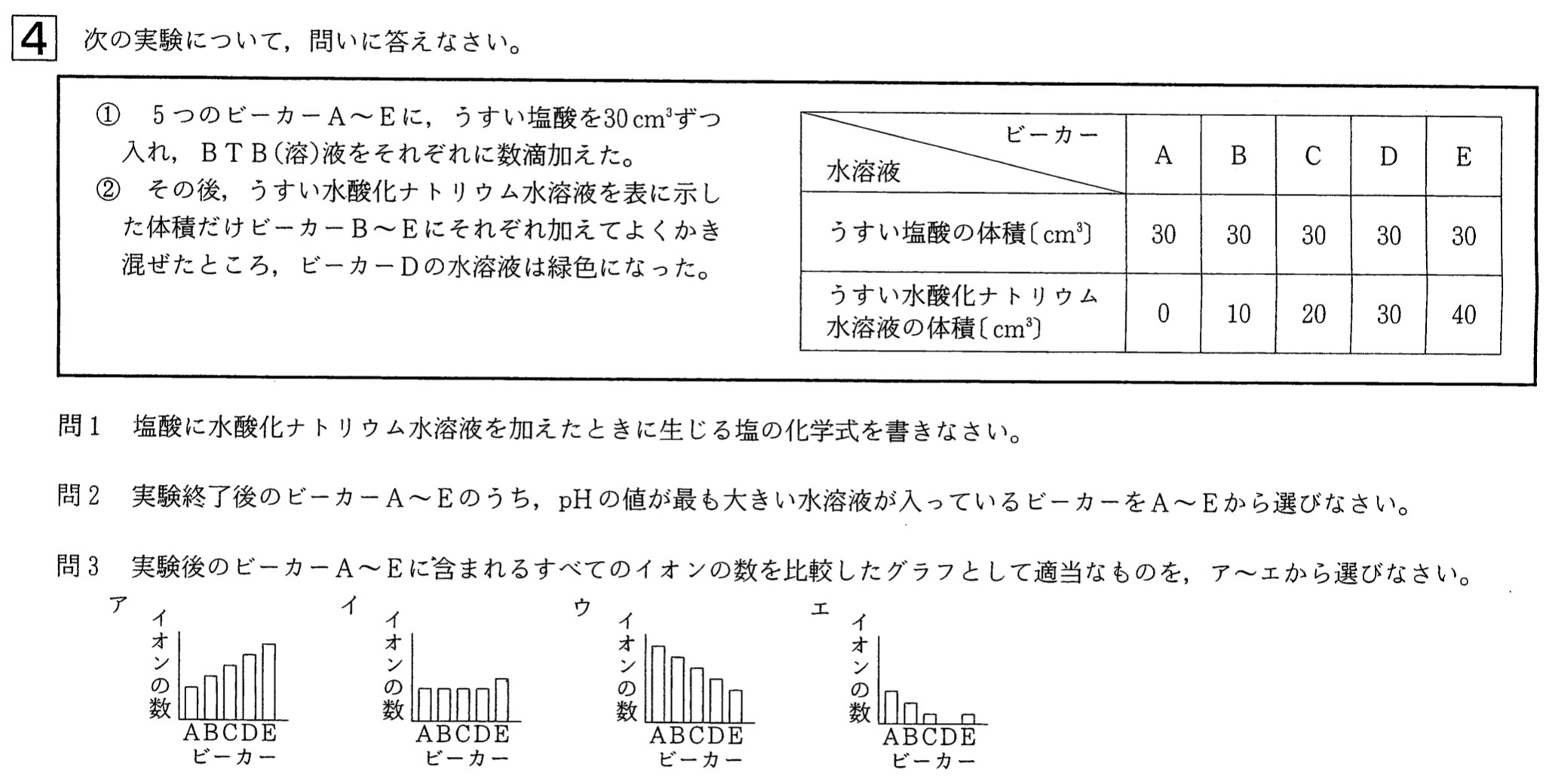
大問4 中和とイオン数
問1
解答:NaCl
解説:
酸である塩酸にアルカリである水酸化ナトリウム水溶液を加えたときの化学反応式は、以下のとおりです。
HCl+NaOH→NaCl+H2O
酸とアルカリが反応して中和が起こると塩と水が生じますが、この場合は塩としてNaClが生じます。
問2
解答:E
解説:
表より、うすい塩酸30cm3とうすい水酸化ナトリウム水溶液30cm3が反応すると、完全に中和されて、塩化ナトリウム水溶液(食塩水)のみになることが分かります。
すなわち、うすい塩酸10cm3に水素イオンH+が1個、うすい水酸化ナトリウム水溶液10cm3に水酸化物イオンOH–が1個あると考えることができます。
これを元に、ビーカーA〜Eにおいて、H+またはOH–が何個あるかを調べて、水溶液のpHを判断していきます。
ビーカーA:H+が3個あるので、水溶液は酸性です。
ビーカーB:H+が2個あるので水溶液は酸性ですが、ビーカーAよりpHは7に近づきます。
ビーカーC:H+が1個あるので水溶液は酸性ですが、ビーカーBよりpHは7に近づきます。
ビーカーD:中性の水溶液で、pHは7です。
ビーカーE:H+が1個あるので水溶液は酸性ですが、pHは7よりやや多い程度と推測できます。
これより、ビーカーEが最もpHが大きいと推測できます。
問3
解答:イ
解説:
中和が起こる間は、水溶液中のイオン数は変化しません。
ビーカーA〜Dでは中和が起こっており、水溶液中のイオン数は変化しません。
ビーカーEでは加えた水酸化ナトリウム水溶液10cm3に含まれるナトリウムイオンNa+と水酸化物イオンOH–の分だけ水溶液中のイオン数は増加します。
以上より、選択肢イが正解です。
大問5 動滑車と定滑車の仕事率 ★問4がやや難
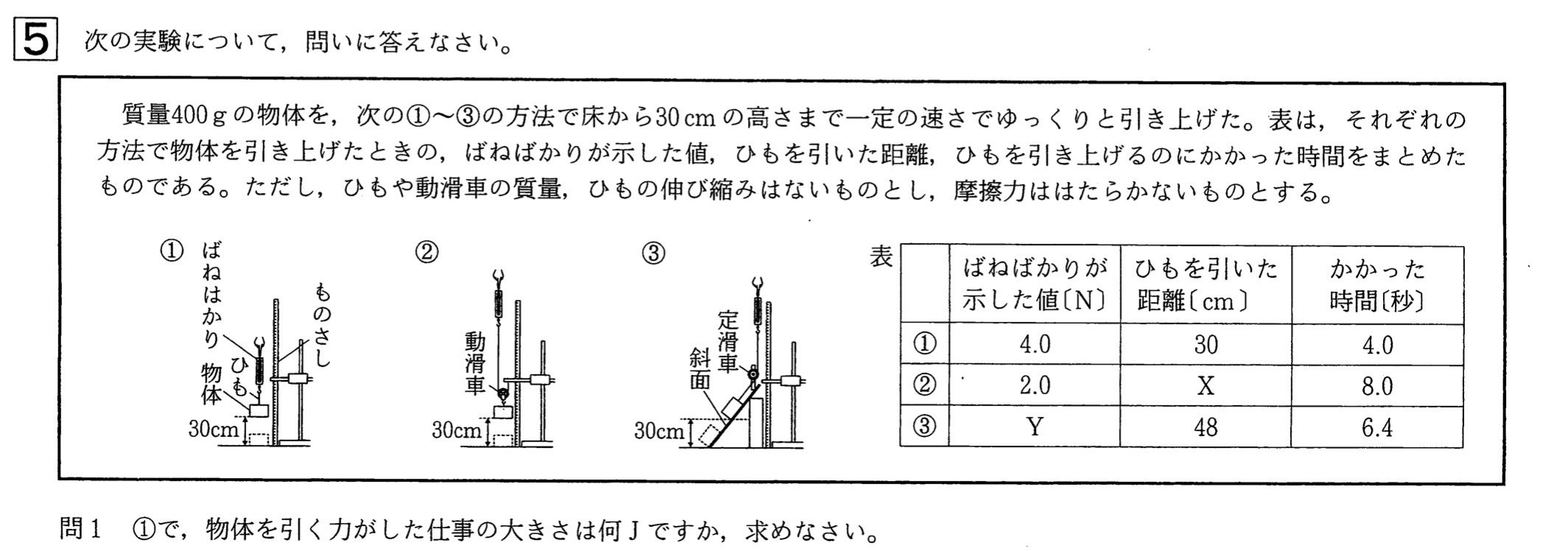

問1
解答:1.2(J)
解説:
仕事の大きさ[J]=加えた力[N]×動かした距離[m]
問題文に「30cmの高さまで一定の速さでゆっくりと引き上げた」とあるので、物体は等速直線運動をしており、加えた力は物体にはたらく重力の大きさと見なすことができます。よって、仕事の大きさは、
仕事の大きさ[J]=加えた力[N]×動かした距離[m]=物体にはたらく重力の大きさ[N]×動かした距離[m]=ばねばかりが示した値[N]×動かした距離[m]=4.0N×0.3m=1.2J
問2
解答:仕事の原理
解説:
単純な知識問題なので、解説略。
問3
解答:X・・・60、Y・・・2.5
解説:
・X
物体を動滑車で引いているので、2本の糸で物体を持ち上げている状態なので、糸1本当たりのおもりを引き上げる力は、物体の重さの半分になります。
実験①より物体の重さは4.0Nであるので、実験②でのばねばかりが示した値は4.0N×1/2=2.0Nです。
・Y
斜面は直角三角形で、斜辺の長さが48cm、高さが30cmなので、物体にはたらく重力の斜面方向の分力を相似を用いて求めると、
4.0N×30/48=30/12=5/2=2.5N
問4 ★やや難
解答:①>③>②
解説:
仕事の原理より、物体を30cmの高さまで持ち上げるのに要した仕事の大きさ[J]は全て同じです。
仕事率の単位[J/s]から、仕事率は仕事をするのにかかった時間[s]に反比例します。実験①〜③でかかった時間は①<③<②の順であるので、仕事率の大きさは①>③>②の順になります。
大問6 動物の分類

問1
解答:胎生
解説:
Xはホニュウ類、Yのハトは鳥類、Yのイモリは両生類です。
仲間の増え方は、ホニュウ類は胎生です。
問2
解答:①・・・ウ、②・・・イ、③・・・ウ
解説:
イモリは両生類だと分かったら、後は両生類の特徴の知識を用いて解くだけです。
※イモリとヤモリの違いについて。イモリは両生類は、「イりょう」とゴロで覚えるとよいです。消去法で、ヤモリはハチュウ類です。
問3
解答:①・・・外骨格、②・・・節足(動物)
解説:
単純な知識問題なので、解説略。
問4
解答:食物連鎖
解説:
単純な知識問題なので、解説略。
大問7 分解後のアミノ酸の排出の流れ
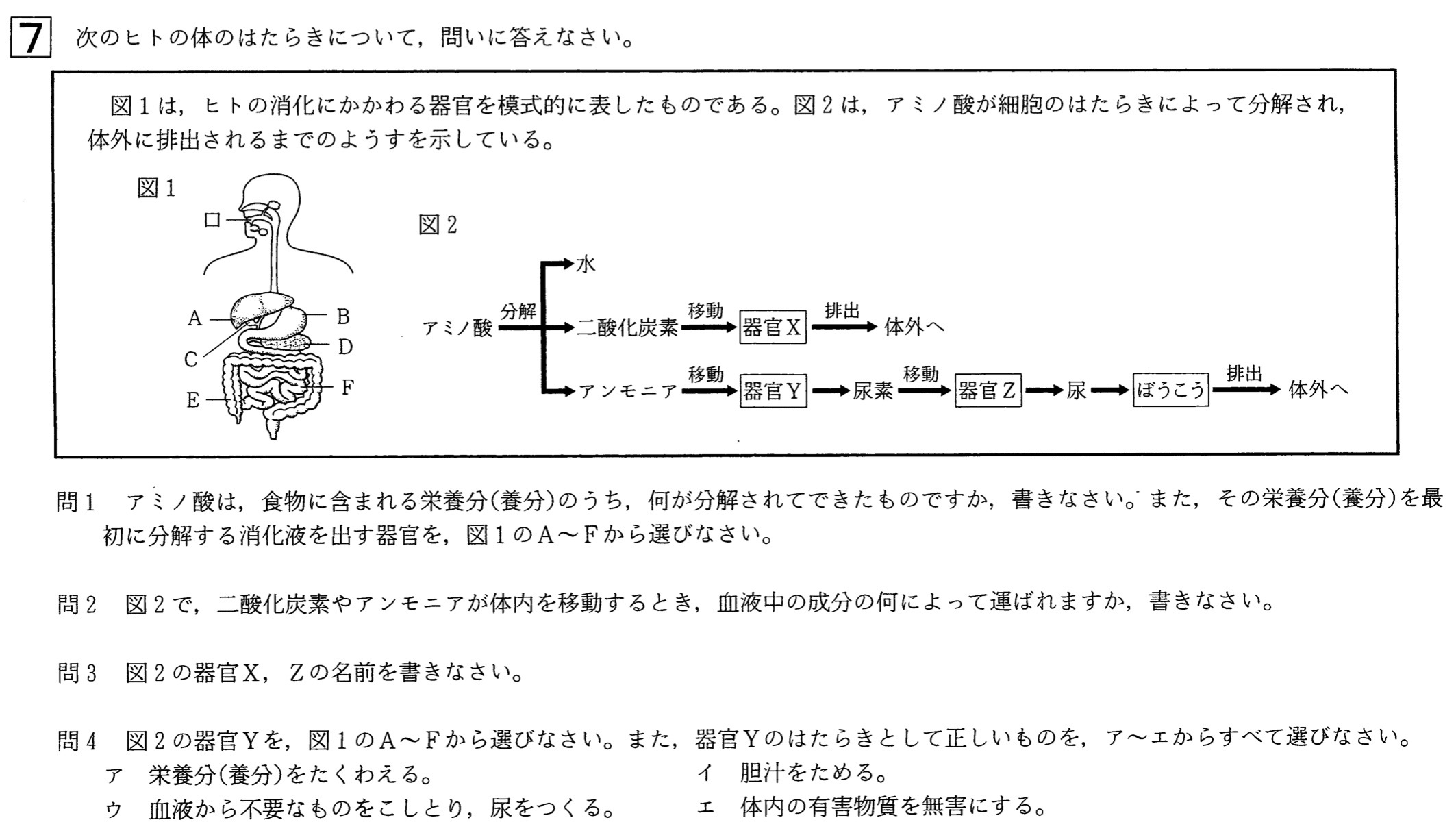
問1
解答:栄養分・・・タンパク質、器官・・・B
解説:
アミノ酸はタンパク質が分解されてできたものです。
タンパク質は、消化液である胃液(B)に含まれる消化酵素ペプシン、消化液であるすい液に含まれる消化酵素トリプシン(D)、小腸(F)の壁から分泌される消化酵素によって、アミノ酸に分解されます。
問2
解答:血しょう
解説:
細胞呼吸で生じた不要物は、細胞間を満たしている組織液を通って血液中の血しょうに取り込まれ、体循環と肺循環によって体外に排出されます。
問3
解答:X・・・肺、Z・・・じん臓
解説:
・X
細胞呼吸によって生じた二酸化炭素が排出される場所は、肺にある肺胞を取り巻く毛細血管です。問われているのは器官なので、肺が答えです。
・Z
細胞呼吸によって生じたアンモニアは肝臓(器官Y)に運ばれて無害な尿素に変えられ、じん臓(器官Z)に運ばれて尿として排出されます。
問4
解答:Y・・・A、はたらき・・・ア、エ
解説:
器官Yは肝臓で、図1ではAに該当します。
肝臓はブドウ糖をグリコーゲンという養分に変換して蓄えたり、脂肪を細かくするだけのはたらきをする胆汁をつくったり、アンモニアを無毒の尿素にするなど体内の有害物質を無害にするはたらきをします。
大問8 柱状図の標高の計算
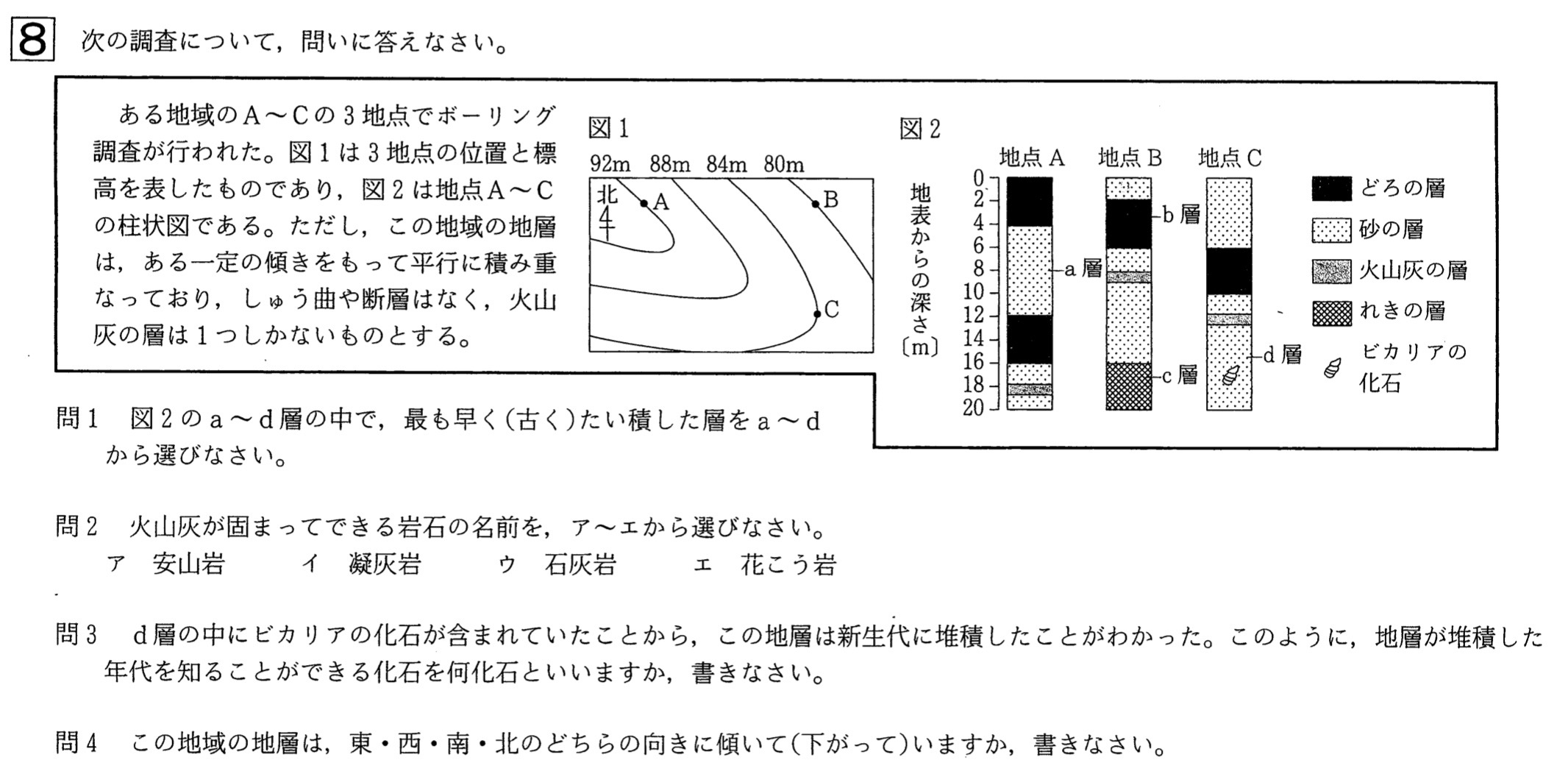
問1
解答:c
解説:
火山灰の層を基準にして調べると、c層→b層→a層の順に堆積したと考えられます。
問2
解答:イ
解説:
単純な知識問題なので、解説略。
問3
解答:示準(化石)
解説:
単純な知識問題なので、解説略。
問4
解答:東
解説:
地点A〜Cの火山灰の層の上面の標高を調べていきます。
・地点A:92m-18m=74m
・地点B:80m-8m=72m
・地点C:84m-12m=72m
地点Bと地点Cの火山灰の層の上面の標高が等しいので、南北方向に水平であることが分かります。
地点Aは地点Bよりも火山灰の層の上面の標高が高いので、西から東に向けて下がっています。
大問9 遺伝 ★問4がやや難

問1
解答:対立形質
解説:
単純な知識問題なので、解説略。
問2
解答:①・・・A、②・・・Aa
解説:
①:丸い種子をつくる純系のエンドウの遺伝子型はAAで、その生殖細胞は分離の法則より、Aです。
②:AA×aa→Aa、Aa、Aa、Aaより、子は全て丸形の種子で、遺伝子型はすべてAaです。
問3
解答:4分の1
解説:
親の代の交配パターンは、AA×aa→Aa、Aa、Aa、Aaです。
子の代の交配パターンは自家受粉していることから、Aa×Aa→AA、Aa、Aa、aaです。
これより、AA:Aa:aa=1:2:1となることから、丸い種子をつくる純系AAのエンドウの体細胞と同じ遺伝子をもつものは、孫全体の4分の1になります。
問4 ★やや難
解答:Aaとaa
解説:
子に丸としわの種子が出現したことから、片親の遺伝子型はAaです。
また、丸:しわ=1:1であったことから、遺伝子の組み合わせは以下のとおりになります。
Aa×aa→Aa、Aa、aa、aa
Aa(丸):aa(しわ)=2:2=1:1
以上より、親がもつ遺伝子の組み合わせは、Aaとaaです。
大問10 太陽の年周運動と星座 ★問3がやや難
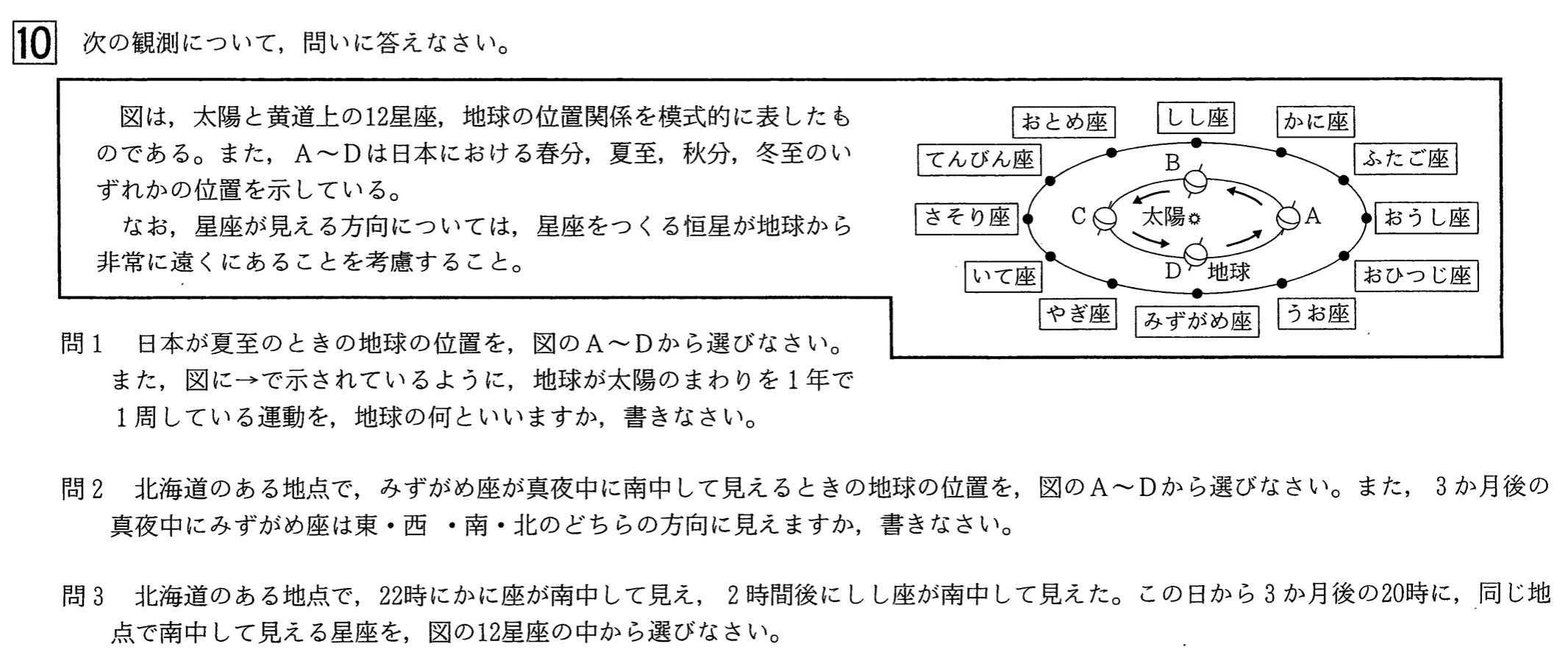
問1
解答:地球の位置・・・C、地球の運動・・・(地球の)公転
解説:
地軸の北極側を太陽に傾けているとき夏至(C)で、地軸の北極側を太陽と反対方向に傾けているとき冬至(A)です。
地球が太陽の周りを反時計回り(西から東)に1年(365日)で1周(360°回転)する運動を、地球の公転といいます。
問2
解答:地球の位置・・・D、3ヶ月後・・・西
解説:
真夜中に南中したことから星座は地球をはさんで太陽と反対方向にあるので、地球は秋分であるDの位置にあります。
3ヶ月=1/4年より、地球は360°×1/4=90°反時計回りに公転するので、3ヶ月後にはAの位置にあります。このときみずがめ座は、真夜中西の空の方向に見えます。
問3 ★やや難
解答:おとめ座
解説:
問題文の条件より、真夜中にしし座が南中したので、地球は春分である地点Bの位置にあります。
この日から3ヶ月後には地球は夏至である地点Cの位置にあり、真夜中にさそり座が南中します。よって、その4時間前の20時に南中する星座を調べればよいので、てんびん座またはおとめ座が該当します。
ここで問題文の条件より、南中する星座は2時間で1つ切り替わるので、4時間では2つ切り替わります。
地球は反時計回りに自転しているので、夏至である地点Cの位置で真夜中にさそり座が南中したので、その4時間前の20時に南中する星座は、さそり座から時計回りに2つ分の位置にあるおとめ座です。